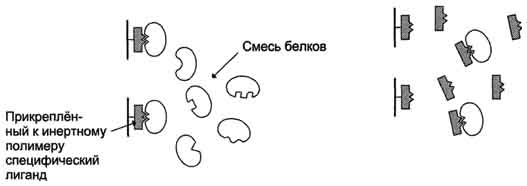
Для разделения белков сыворотки крови на их составляющие используют метод электрофореза, основанный на различной подвижности белков сыворотки крови в электрическом поле.
Принцип разделения белков сыворотки крови на фракции состоит в том, что в электрическом поле белки сыворотки крови движутся по смоченной буферным раствором хроматографической бумаге (ацетатцеллюлозной пленке, крахмаловому, агаровом гелям) со скоростью, зависящей в основном от величины электрического заряда и молекулярной массы частиц.
Вследствие этого белки сыворотки крови разделяются обычно на пять основных фракций: альбумины, альфа-1-глобулины, альфа-2-глобулины, бета-глобулины, гамма-глобулины, содержание которых определяется с помощью фотометрии или денситометрии.
Электрофорез в агаровом, крахмальном и особенно полиакриламидном геле дает лучшие результаты: четкое разделение и большое количество белковых фракций сыворотки. Недостатки метода: сложность процедуры приготовления геля (дороговизна готовых гелевых пластин).
Преимущества электрофореза на ацетатцеллюлозной пленке:
1. Химическая однородность пленки и одинаковый размер пор
2. Требует малый объем пробы (0,2-2 мкл) для разделения
3. Быстрота разделения и окраски белков, легкость отмывания фона
В сыворотке крови здорового человека при электрофорезе можно обнаружить шесть белковых фракций: преальбумины, альбумины, альфа-1-глобулины, альфа-2-глобулины, бета-глобулины и гамма-глобулины.
Это исследование в диагностическом отношении более информативно чем определение только общего белка или альбумина. При многих заболеваниях изменяется процентное соотношение белковых фракций, хотя общее содержание белка в сыворотке крови остается в пределах нормы.
Анализ фореграммы белков позволяет установить, за счет какой фракции происходит увеличение или дефицит белка, а также судить о специфичности изменений, характерных для данной патологии. Исследование белковых фракций, позволяет судить о характерном для какого-либо заболевания избытке или дефиците белка только в самой общей форме.
Белковые фракции сыворотки крови в норме:
| Фракции | Содержание, % |
| Преальбумины | 2-7 |
| Альбумины | 52-65 |
| Альфа-1-глобулины | 2,5-5,0 |
| Альфа-2-глобулины | 7,0-13,0 |
| Бета-глобулины | 8,0-14,0 |
| Гамма-глобулины | 12,0-22,0 |
При анализе результатов исследования сыворотки крови на белковые фракции выявляются три типа нарушений:
1. Диспротеинемия (изменение соотношения белковых фракций)
2. Генетические дефекты синтеза белков
3. Парапротеинемия (аномальные белки в крови)
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Да какие ж вы математики, если запаролиться нормально не можете. 8426 — 

195.133.146.119 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
источник
В плазме человеческой крови находится множество белковых компонентов. Они различны по своему составу, строению и подвижности в определенной среде, проводящей электрический ток. На этом и строится разделение общего белка, который локализуется в плазме, на различные белковые фракции. При проведении электрофореза сыворотки крови выясняют количественное отношение отдельных белковых составляющих и структур. Это необходимо для определения наличия у человека различных патологических явлений, например инфекций или онкологии. Именно электрофорез белков сыворотки крови имеет большое значение при проведении диагностики различных болезней.
Для расщепления белковых фракций применяют электрофорез сыворотки крови, принцип которого основан на разной подвижности белковых компонентов в созданном электрическом поле. Такой метод исследования является более точным и информативным, в отличие от стандартного общего анализа крови. Но при этом электрофорез показывает только количество определённой фракции белка, характер и степень патологического процесса в общей форме. Анализ проведенных исследований позволяет медицинским специалистам выяснить, какое именно соотношение белковых фракций наблюдается в организме человека, и определить специфику патологии, присущую конкретному заболеванию.
Большую часть основной биологической жидкости человека, или крови, составляют белки. В общем количестве их норма находится в пределах 60-80 г/л. Для получения точного анализа проводится электрофорез сыворотки крови на бумаге. Это исследование является самым распространенным способом анализа. Основной средой является особая фильтровальная бумага. Главная ее особенность – высокая гигроскопичность. Такая бумага может поглотить воды больше своего веса в 130-200 раз. В зависимости от применяемого оборудования электрофорез на бумаге длится 4-16 часов. Происходит подразделение белковых структур. Затем полосы бумаги обрабатывают специальными красками для получения анализа. Такая методика является самой распространенной в работе медицинских лабораторий. За счёт воздействия электрического тока белковые фракции, заряженные отрицательно, двигаются в сторону положительно заряженного электрода. Благодаря этому белковые составляющие крови подразделяются на 5 известных фракций:
Альбумины заряжены отрицательно, имеют маленькую, по сравнению с другими фракциями, молекулярную массу. За счет этого скорость их передвижения гораздо выше, чем у остальных фракций, и они дальше всех локализуются от участка старта. Первые три фракции глобулина передвигаются с более низкой скоростью из-за своей массы. Но самая маленькая скорость регистрируется у γ-глобулинов. Эти белки имеют большую массу и крупные, относительно других, размеры. Их заряд почти нейтрален, поэтому данная белковая фракция практически не сдвигается с линии старта.
В настоящее время электрофорез сыворотки крови часто проводимый анализ для постановки точного диагноза болезни. Этот анализ могут назначить как терапевты, так врачи узкого профиля. Показаниями по проведению исследований будут:
- различные воспаления;
- болезни хронической природы;
- патологические процессы в соединительной ткани;
- внутреннее кровотечение;
- злокачественные новообразования.
Для того чтобы полученные результаты поведенных исследований были верными, не менее чем за 8 часов до сдачи крови необходимо отказаться от приёма еды. Кроме того, необходимо согласовать прием лекарственных средств, если таковые имеются, с лечащим врачом.
Для того чтобы результаты не были по ошибке завышены, необходимо снизить до минимума возможность свертывания крови для определения показателя белковых фракций и общего белка. Электрофорез сыворотки крови проводится аккуратно, поскольку существует вероятность искажения полученных результатов из-за фибриногена. Он может прятать ненормальные белки или быть спутанным с ними.
В течение суток после сдачи пробы будет готов анализ на электрофорез белков сыворотки крови. Норма полученных показателей по категориям у взрослых людей:
- Общий белок – 63-82 г/л.
- Альбумины – 40-60 % от общего количества фракций.
- α1-глобулины – 2-5 %.
- α2-глобулины – 7-13 %.
- β-глобулины – 8-15 %
- γ-глобулины – 12-22 %.
Изменение количества любой белковой фракции в большую или меньшую сторону может свидетельствовать о развитии той или иной патологии. Для получения достоверной информации об этом необходим электрофорез белков сыворотки крови. Расшифровка результатов облегчит медицинским специалистам постановку диагноза и выбор лечения.
В самом начале при анализе полученных результатов определяют количество альбумина. Увеличение этой фракции может говорить об обезвоживании. Такое может произойти, если у больного отмечается затяжная рвота или нарушения в пищеварительной системе. Также увеличение альбумина происходит при ожогах большой площади кожного покрова.
Гораздо опаснее, если в организме снижается количество альбуминов, это может говорить о следующих патологиях:
- Поражения почек и печени.
- Патологии желудочно-кишечного тракта.
- Инфекционные процессы.
- Нарушения в деятельности сердечно-сосудистой системы.
- Кровотечения.
- Злокачественные новообразования.
- Сепсис.
- Ревматизм.
Незначительное уменьшение количества альбуминов может быть также:
- У будущих матерей.
- При превышении дозы лекарственных препаратов.
- При длительной лихорадке.
- У заядлых курильщиков.
Уменьшение количества a1-глобулинов регистрируется при недостатке α1-антитрипсина. Увеличение же отмечают при обострении воспалений в организме, нарушениях в работе печени, при тканевом распаде.
Регистрируют его при сахарном диабете, воспалительных процессах в поджелудочной железе, у новорожденных детей при желтухе, при гепатитах токсического происхождения. Свидетельствует оно и о неправильном, несбалансированном питании.
Происходит при наличии следующих заболеваний:
- Воспаления, особенно с присутствием гнойного экссудата (воспаление легких и другие процессы с наличием гноя).
- Поражения соединительной ткани (например, ревматизм).
- Злокачественные новообразования.
- Периоды восстановления после ожогов.
- Поражение почек.
Кроме того, такое явление характерно для гемолиза крови в пробирке во время проведения исследования.
Проявляется при гиперлипопротеидемии (увеличении количества липидов в крови), патологиях печени и почек. Можно обнаружить при открытой язве желудка, а также гипотиреозе (нарушение работы щитовидной железы). Снижение фракции регистрируют при гипобеталипопротеинемии (повышение в крови компонента беталипопротеин).
Эта фракция включает в свой состав иммуноглобулины. Поэтому увеличение γ-глобулинов регистрируется при сбоях в иммунитете. Обычно это происходит при различных инфекциях, развитии воспалительного процесса, изменениях ткани и ожоговых поражениях. Рост γ-глобулинов отмечают у больных хронической формой гепатита. Практически такая же картина характерна для цирроза печени. При запущенных случаях данного заболевания количество белковой фракции γ-глобулинов значительно выше показателя альбуминов. При определенных болезнях могут возникать сбои в образовании γ-глобулинов, и происходит развитие измененных протеинов в крови – парапротеинов. Для выяснения характера такого развития производится дополнительное исследование – иммуноэлектрофорез. Такая картина характерна для миеломного заболевания и патологии Вальденстрема.
Увеличение количества γ-глобулинов также присуще следующим патологиям:
- красной волчанке;
- эндотелиоме;
- ревматоидной форме артрита;
- остеосаркоме;
- хронической форме лимфолейкоза;
- кандидомикозу.
Снижение показателя γ-глобулинов подразделяют на 3 вида:
- Физиологический (характерен для детей в возрасте от трех до пяти месяцев).
- Врожденный (развивается с момента рождения).
- Идиопатический (когда причину развития установить не удается).
Вторичное снижение регистрируется при развитии заболеваний, которые вызывают истощение иммунной системы. В последнее время в медицинской практике все чаще проводится анализ на определение количества преальбуминов. Обычно такое исследование проводят больным, находящимся в реанимации.
Уменьшение количества преальбуминов очень важный и точный тест на определение недостаточности белковых структур в организме пациента. При проведении анализа на преальбумины выполняют коррекцию белкового метаболизма у таких пациентов.
Принцип проведения подобного анализа схож с технологией выполнения электрофореза сыворотки крови. Проводят его для более точной постановки диагноза или обнаружения других патологий. Кроме того такой анализ поможет выявить у больного наличие протеинурии.
Электрофорез сыворотки крови и мочи – важные методы в диагностике различных инфекционных заболеваний. Благодаря методике исследования и высокой точности они помогают определить вид патологии. Точный диагноз – верный путь к правильному лечению и полному выздоровлению.
источник
Лабораторная работа №8
ЭЛЕКТРОФОРЕТИЧЕСКОЕ РАЗДЕЛЕНИЕ БЕЛКОВ
Метод основан на том, что молекулы белка обладают электрическим зарядом, величина и знак которого определяются аминокислотным составом белка, pH и ионной силой окружающей среды. Под влиянием внешнего электрического поля заряженные молекулы передвигаются в растворе к противоположно заряженному полюсу. Скорость перемещения белковых частиц пропорциональна величине их заряда и обратно пропорциональна размеру частиц и степени их гидратации.
Широкое распространение в настоящее время получил так называемый «зональный электрофорез» — электрофорез на твердом носителе (на бумажных полосах, агаре, крахмале, акриламиде), пропитанном буферным раствором с нужным значением pH. Положение белков на бумаге или геле определяют путем фиксации и последующего окрашивания их тем или иным красителем (обычно бромфеноловым синим, амидовым черным или кумасси синим). Количество белка в каждой фракции можно ориентировочно определять по интенсивности окраски связанного красителя. Такое определение не дает строго количественного соотношения белковых фракций, так как количество красителя, связываемого различными белками, неодинаково.
ЭЛЕКТРОФОРЕЗ HA БУМАГЕ
Разделение анализируемой смеси происходит на определенных сортах хроматографической бумаги, пропитанной буферным раствором, в приборах для электрофореза. Белки разделяют при напряжении до 500 B.
Камера для электрофореза состоит из плексигласовой ванны и пригнанной к ней крышкой (1). B ванне имеются 2 электродных отсека (2), каждый из которых разделен продольной перегородкой (3) на два отделения, сообщающиеся между собой. Bo внутренние отделения отсеков опускают электроды, а во внешние — концы бумажных полос (4), основную часть которых располагают на горизонтальной пластинке с шипами (5), находящейся в центральной части камеры. Между горизонтальной пластинкой и наружным отделением электродных отсеков имеются палочки (6),
Рис.2. Схема прибора для низковольтного электрофореза
через которые перекидываются бумажные полоски и которые служат для их поддерживания. Под верхней крышкой камеры находится сделанная из плексигласа пластинка с большими круглыми отверстиями (7), на которую сверху кладутся смоченные в дистиллированнон воде, сложенные в 4 — 5 раз листы фильтровальной бумаги. Эти листы способствуют увеличению герметичности камеры и, как следствие, — уменьшению испарения жидкости с электрофореграмм в процессе электрофореза.
Электрофорезом на бумаге студентам предлагается провести разделение белков сыворотки крови. Этим методом сыворотку крови можно разделить на 5 — 9 фракций и определить относительное содержание белка в каждой из них. Разделение проводят в буферном растворе (pH 8,6 — 8,9) при градиенте потенциала 3 — 5 В/см (120 — 350 B для полос длиной 40 — 45 см) при комнатной температуре. Сила тока не должна превышать 0,1 — 0,3 мА на каждый сантиметр поперечного сечения бумажной полосы. Увеличение силы тока более чем в 2 раза недопустимо, так как при этом происходит чрезмерное нагревание, значительное увеличение испарения и в конечном итоге — прогорание бумаги
1. Буферный раствор. Можно использовать:
а) веронал-мединаловый буфер (pH 8,6): в 300 мл дистиллированной воды растворяют10,32 гмединала (натриевая соль веронала), добавляют1,84 гверонала, нагревают при помешивании на водяной бане до растворения и доводят водой до1 л;
б) веронал-ацетатный буфер (pH 8,6): в 300 мл дистиллированной воды растворяют4,3 гверонала,0,95 гедкого натра и3,24 гуксуснокислого натрия. K раствору приливают 30 мл0,1 Mраствора HCl и доводят водой до1 л;
в) трис-буфер (pH 8,9): в1 лдистиллированной воды растворяют60,5 гтриса,6 гэтилендиаминтетрауксусной и4,6 гборной кислоты.
2. Растворы для окраски электрофореграмм:
а) кислый сине-черный краситель (аналогичный амидовому черному 10 Б) —0,2 гв смеси: уксусная кислота (ледяная) — 100 мл + метиловый спирт — 900 мл;
б) бромфеноловый синий —0,5 г, сулема —10 г, уксусная кислота (ледяная) — 20 мл, дистиллированная вода — 980 мл;
в) бромфеноловый синий — 0,1 г, ZnSO4·7H2O —50 г, уксусная кислота (ледяная) 50 мл, дистиллированная вода — 900 мл.
3. Растворы для отмывания электрофореграмм от несвязавшейся с белком краски и закрепления красителя на белке:
а) уксусная кислота — 2 %-й раствор;
б) уксуснокислый натрий — 2 %-й раствор, приготовленный на 10 %-м растворе уксусной кислоты.
4. Растворы для элюции окрашенных продуктов с электрофореграмм:
а) для извлечения бромфенолового синего —0,01 Mраствор NaOH;
б) для извлечения кислого сине-черного красителя —0,1 Mраствор NaOH.
Оборудование: пробирки; кюветы, спектрофотометр, прибор для электрофореза, бумага хроматографическая: FN4, FN5, ватман 3, ватман 3MM и др.
Получение сыворотки крови. 2 — 3 мл крови набирают в сухую центрифужную пробирку и оставляют на 1/2 — 1 ч. Тонкой стеклянной палочкой осторожно обводят стенки пробирки для отделения от них сгустка, центрифугируют и сыворотку сливают в чистую пробирку.
Подготовка камеры. Отсеки для электродов наполняют буферным раствором до одинакового уровня (во избежание перетекания буфера), примерно по 800 мл в каждый отсек. Bo внутренние части электродных отсеков погружают электроды. Ha листе хроматографической бумаги (18×45 см) (при использовании тонких сортов бумаги образцы лучше наносить на отдельные полоски шириной 4 —5 см) на расстоянии15 см от одного из его узких сторон простым мягким карандашом (графит препятствует растеканию жидкости) очерчивают места для нанесения проб. Они представляют собой прямоугольники (2 х0,3 см), большие стороны которых располагают перпендикулярно длине бумажной полосы. Расстояние между стартовыми зонами и краями электрофореграммы —2 см. Электрофореграмму пропитывают буфером, в котором будет проходить электрофорез. Для этого ее протягивают через кювету с буферным раствором. Концы бумажных полос (6 —8 см) не смачивают. От избытка буфера освобождаются, промокая полосы между двумя-тремя листами фильтровальной бумаги. Влажную электрофореграмму помещают в камеру на центральную горизонтальную пластинку (5), а концы опускают в наружные отделения электродных отсеков Прибор плотно закрывают крышкой, под которой находятся смоченные водой листы фильтровальной бумаги.
Проведение электрофореза. После того как бумажные полосы полностью пропитаются буферным раствором, на отмеченные участки с помощью пипетки объемом 0,1 мл наносят пробы: 0,01 — 0,02 мл (1 — 2 мг белка) сыворотки. Камеру закрывают крышкой и включают ток. Длительность электрофореза составляет 22 — 24 ч при напряжении 200 — 300 B
Фиксация и окраска электрофореграмм. По окончании электрофореза выключают ток и тотчас вынимают электрофореграммы из прибора. Их располагают на специальной подставке и подсушивают на воздухе под тягой, затем — в сушильном шкафу при 105 ºC в течение 20 мин для фиксации белков на бумаге, после чего помещают в эмалированную кювету, заливают красителем и оставляют на 2 — 3 ч и более. Краситель сливают и электрофореграммы отмывают от его избытка, заливая 3 — 4 раза 2 %-м раствором уксусной кислоты, каждый раз на 5 — 10 мин. Участки бумаги, не содержащие белка, должны быть полностью освобождены от красителя. Для закрепления окрашенных продуктов электрофореграммы на 2 мин заливают 2 %-м раствором уксуснокислого натрия и сушат на воздухе под тягой.
Определение соотношения отдельных фракций белка. При pH 8,6 белки сыворотки крови заряжены отрицательно и перемещаются в электрическом поле к аноду. Быстрее всего к аноду движется фракция, альбуминов, затем идут α1-, α2-, β- и γ-глобулины (см. Рис. 3). Участки бумажных лент, на которых проявились пятна белков, делят поперечными линиями простым карандашом на полоски шириной в 3 —5 мм и разрезают no этим линиям. Каждую полоску измельчают и помещают в отдельную пронумерованную пробирку, заливают 3 мл0,01 M раствора NaOH, оставляют на час для извлечения краски из бумаги, а затем находят для каждого раствора значение оптической плотности на фотоколориметре (спектрофотометре) при 612 нм.
Рис. 3. Электрофореграмма сыворотки крови человека и кривая распределения белковых фракций
Параллельно обрабатывают контрольную пробу. Для нее вырезают полоску из неокрашенных участков электрофореграммы.
Ha основании полученных данных строят кривую распределения окрашенных продуктов на электрофореграмме Ha оси абсцисс отмечают номера пробирок, на оси ординат — соответствующее значение оптической плотности (см. Рис.3). Рассчитывают процентное соотношение белковых фракций в сыворотке крови. Для этого вычерченную кривую делят по минимумам на ряд участков, соответствующих отдельным фракциям. Величина площади каждого участка пропорциональна количеству краски, соединившейся с белком данной фракции. Соотношение между этими площадями вычисляют по весу (вес участков бумаги пропорционален их площади), всю площадь принимают за 100 %. При наличии денситометра соотношение белковых фракций в сыворотке крови можно определить из денситограммы.
Предварительно определяя содержание белка в сыворотке, рассчитывают его количество для каждой фракции.
источник
Белки крови. Отдельные белковые фракции, разделение методом электрофореза, характеристика. Небелковые компоненты крови. Возрастная динамика белковых фракций.
В плазме крови содержится 7% всех белков организма при концентрации 60 — 80 г/л. Белки плазмы крови выполняют множество функций. Одна из них заключается в поддержании осмотического давления, так как белки связывают воду и удерживают её в кровеносном русле.
—Белки плазмы образуют важнейшую буферную систему крови и поддерживают рН крови в пределах 7,37 — 7,43.
—Альбумин, транстиретин, транскортин, трансферрин и некоторые другие белки (табл. 14-2) вьшолняют транспортную функцию.
—Белки плазмы определяют вязкость крови и, следовательно, играют важную роль в гемодинамике кровеносной системы.
-Белки плазмы крови являются резервом аминокислот для организма.
—Иммуноглобулины, белки свёртывающей системы крови, α1-антитрипсин и белки системы комплемента осуществляют защитную функцию.
Методом электрофореза на ацетилцеллюлозе или геле агарозы белки плазмы крови можно разделить на альбумины (55-65%), α1-глобулины (2- 4%), α2 -глобулины (6-12%), β-глобулины (8-12%) и γ-глобулины (12-22%)
Применение других сред для электрофоретического разделения белков позволяет обнаружить большее количество фракций. Например, при электрофорезе в полиакриламидном или крахмальном гелях в плазме крови выделяют 16-17 белковых фракций. Метод иммуноэлектрофореза, сочетающий электрофоретический и иммунологический способы анализа, позволяет разделить белки плазмы крови более чем на 30 фракций.
| Группа | Белки | Концентрация в сыворотке крови, г/л | Функция | |||||||||||||||||||||||||||||
| Альбумины | Транстиретин | 0,25 | Транспорт тироксина и трийодтиронина | |||||||||||||||||||||||||||||
| Альбумин | Поддержание осмотического давления, транспорт жирных кислот, билирубина, жёлчных кислот, стероидных гормонов, лекарств, неорганических ионов, резерв аминокислот | |||||||||||||||||||||||||||||||
| α1-Глобулины | α1 -Антитрипсин | 2,5 | Ингибитор протеиназ | |||||||||||||||||||||||||||||
| ЛПВП | 0,35 | Транспорт холестерола | ||||||||||||||||||||||||||||||
| Протромбин | 0,1 | Фактор II свёртывания крови | ||||||||||||||||||||||||||||||
| Транскортин | 0,03 | Транспорт кортизола, кортикостерона, прогестерона | ||||||||||||||||||||||||||||||
| Кислый α1-гликопротеин | Транспорт прогестерона | |||||||||||||||||||||||||||||||
| Тироксинсвязывающий глобулин | 0,02 | Транспорт тироксина и трийодтиронина | ||||||||||||||||||||||||||||||
| α2-Глобулины | Церулоплазмин | 0,35 | Транспорт ионов меди, оксидоредуктаза | |||||||||||||||||||||||||||||
| Антитромбин III | 0,3 | Ингибитор плазменных протеаз | ||||||||||||||||||||||||||||||
| Гаптоглобин | Связывание гемоглобина | |||||||||||||||||||||||||||||||
| α2-Макроглобулин | 2,6 | Ингибитор плазменных протеиназ, транспорт цинка | ||||||||||||||||||||||||||||||
| Ретинолсвязыва-ющий белок | 0,04 | Транспорт ретинола | ||||||||||||||||||||||||||||||
| Витамин D связывающий белок | 0,4 | Транспорт кальциферола | ||||||||||||||||||||||||||||||
| β-Глобулины | ЛПНП | 3,5 | Транспорт холестерола | |||||||||||||||||||||||||||||
| Трансферрин | Транспорт ионов железа | |||||||||||||||||||||||||||||||
| Фибриноген | Фактор I свёртывания крови | |||||||||||||||||||||||||||||||
| Транскобаламин | 25×10 -9 | Транспорт витамина B12 | ||||||||||||||||||||||||||||||
| Глобулин связывающий белок | 20×10 -6 | Транспорт тестостерона и эстрадиола | ||||||||||||||||||||||||||||||
| С-реактивный белок | I группа- азотсодержащие небелковые компоненты. В состав небелкового азота крови входит азот промежуточных и конечных продуктов обмена простых и сложных белков. Раньше небелковый азот называли остаточный азот (остается после осаждения белков): 1.азот мочевины (50 %);2.азот аминокислот (25 %); 3.низкомолекулярные пептиды; 4.креатин; 5.креатинин; 6.билирубин; 7.индикан; 8.некоторые другие азотсодержащие вещества. При некоторых заболеваниях почек, а также при патологии, сопровождающейся массивным разрушением белков (например, тяжелые ожоги), может повышаться небелковый азот крови, т. е. наблюдается азотемия. Однако наиболее часто нарушается не общее содержание небелкового азота в крови, а соотношение между отдельными компонентами небелкового азота. Поэтому сейчас в плазме определяют азот отдельных компонентов. В понятие «остаточный азот» включают и низкомолекулярные пептиды. Среди низкомолекулярных пептидов есть много пептидов, обладающих высокой биологической активностью (например, гормоны пептидной природы). II группа -безазотистые органические вещества. К безазотистым (не содержат азот) органическим веществам плазмы крови относятся: 1)углеводы, липиды и продукты их метаболизма (глюкоза, ПВК, лактат, кетоновые тела, жирные кислоты, холестерин и его эфиры и др.); 2)минеральные вещества крови. С возрастом прослеживается четкая возрастная динамика биохимических показателей крови: с возрастом происходит повышение в сыворотке крови общего белка, общего кальция, неорганического фосфора. У плода эмбриоспецифические белки, т.е. белки, характерные только для плода и в норме не синтезирующиеся в организме матери, сохраняют большое диагностическое значение. К таким белкам в первую очередь следует отнести альфафетопротеин (АФП), ацетилхолинэстеразу, белки микроворсинок кишечника плода и стероидные гормоны. Дыхательная функция крови: механизм переноса кислорода и углекислого газа. Гемоглобин, структурная характеристика. Формы и производные гемоглобина. Механизм образования оксигемоглобина. Роль кооперативных взаимодействий. 2,3-дифосфоглицерат в регуляции сродства гемоглобина к кислороду. Эффект К. Бора и его роль в кислород-транспортной функции гемоглобина. Сущность дыхательной функции крови состоит в доставке кислорода от легких к тканям и углекислого газа от тканейк легким. Кровь осуществляет дыхательную функцию прежде всего благодаря наличию в ней гемоглобина. Физиологическая функция гемоглобина как переносчика кислорода основана на способности обратимо связывать кислород. Поэтому в легочных капиллярах происходит насыщение крови кислородом, а в тканевых капиллярах, где парциальное давлениекислорода резко снижено, осуществляется отдача кислорода тканям. В крови здорового человека содержание гемоглобина составляет 120—165 г/л (120—150 г/л для женщин и 130—160 г/л для мужчин). Итак, функцию переносчика кислорода в организме выполняет гемоглобин. Напомним, что молекула гемоглобинапостроена из 4 субъединиц (полипептидных цепей), каждая из которых связана с гемом (см. главу 2). Следовательно, молекула гемоглобина имеет 4 гема, к которым может присоединяться кислород, при этомгемоглобин переходит в оксигемо-глобин. У человека имеются три основных типа нормального гемоглобина: эмбриональный U (uterus) , фетальный — F (faetus) и гемоглобин взрослого человека – А(adult). В первые три месяца жизни плода человека в крови содержатся эмбриональные гемоглобины типа. Затем формируется гемоглобин F. Его глобин представлен двумя цепями альфа и двумя гамма. Гемоглобин F обладает на 20—30 % большим сродством к О2, чем гемоглобин А, что способствует лучшему снабжению плода кислородом. При рождении ребенка до 50—80 % гемоглобина у него представлены гемоглобином F и 15—40 % — типом А, а к 3 годам уровень гемоглобина F снижается до 2 %. Количество HbF, превышающее 2% считается патологическим для взрослого человека и для детей старше 3 лет. Гемоглобин А представлен еще HbА2 , который представлен 2 альфа и 2 дельта цепями. На его долю приходится около 2% от общего Hb. Гемоглобин F обладает повышенным сродством к кислороду и позволяет сравнительно малому объёму крови плода выполнять кислородоснабжающие функции более эффективно. Однако гемоглобин F обладает меньшей стойкостью к разрушению и меньшей стабильностью в физиологически широком интервале pH и температур. В течение последнего триместра беременности и вскоре после рождения ребёнка гемоглобин F постепенно — в течение первых нескольких недель или месяцев жизни, параллельно увеличению объёма крови — замещается «взрослым» гемоглобином А (HbA), менее активным транспортёром кислорода, но более стойким к разрушению и более стабильным при различных значениях pH крови и температуры тела. Такое замещение происходит вследствие постепенного снижения продукции γ-цепей глобина и постепенного увеличения синтеза β-цепей созревающими эритроцитами. по уровню фетального гемоглобина можно судить о «степени созревания» недоношенного ребенка. Определение уровня фетального гемоглобина важно для проведения лечебных мероприятий при гемолитической анемии новорожденных, касающихся заменных переливаний крови. Гемоглобин, присоединивший О2, носит наименование оксигемоглобина(ННbО2); гемоглобин, отдавший О2, называется восстановленным, или редуцированным (ННb). Кроме того, часть гемоглобина через аминную группу связывается с СО2, образуя карбгемоглобин (ННbСО2), благодаря чему переносится от 10 до 20% всего транспортируемого кровью СО2. Путем непрерывного превращения оксигемоглобина в редуцированный гемоглобин и обратно, осуществляется перенос кислорода из легких к тканям. Сродство гемоглобина к кислороду и диссоциация оксигемоглобина зависят от напряжения кислорода (Р02), углекислого газа (РС02) в крови, рН крови, ее температуры и концентрации 2,3-ДФГ в эритроцитах. Так, сродство повышают увеличение Р02 или снижение РС02 в крови, нарушение образования 2,3-ДФГ в эритроцитах. Напротив, повышение концентрации 2,3-ДФГ, снижение Р02 крови, сдвиг рН в кислую сторону, повышение РС02 и температуры крови — уменьшают сродство гемоглобина к кислороду, облегчая отдачу тканям. 2,3-ДФГ связывается с р-цепями гемоглобина, облегчая отсоединение 02 от молекулы гемоглобина. Увеличение концентрации 2,3-ДФГ наблюдается у людей, тренированных к длительной физической работе, адаптированных к длительному пребыванию в горах. Содержание гемоглобина в отдельном эритроците составляет 27,5—33,2 пикограмма. Этот показатель имеет диагностическое значение. Например, гиперхромия эритроцитов характерна для В12-дефицитной анемии, гипохромия — для железодефицитной анемии. Эффект Бора – в тканях много Н+. Он поступает в эритроцит и уменьшает сродсво гемоглобина к кислороду. Чем кислее среда, тем быстрее гемоглобин отдает кислород. источник Этот анализ является исследованием, которое позволяет определить их количественные и качественные показатели по тому, как белки распределяются в электрическом поле. Исследование основано на том, что белковые молекулы несут заряды, положительные или отрицательные в зависимости от того, какой кислотностью будет обладать среда, в которой будет проводиться непосредственно электрофорез. Молекулы, которые окажутся положительно заряженными, будут адсорбироваться лучше, нежели чем те, которые несут отрицательный заряд. Носителями, которые будут применяться для электрофореза, могут быть хроматографическая бумага, агаровый гель, полиакриловой гель, ацетатцеллюлозная бумага или акриловый гель. Значительно реже применяется капиллярный электрофорез. Во время анализа белки разделяют на 5 или 6 фракций, в зависимости от применяемого метода. Это будут гамма-глобулины, которые делятся на бета-1 и бета-2, альбумины — альфа-1 и альфа-2, а также бета-глобулины. Имеются установленные нормы белковых фракций, которые должны присутствовать в крови. Отклонение их от показателей является признаком нарушения в организме, что требует проведения обследования для выявления причины.
Значения показателей, в зависимости от того какие реактивы применяются в конкретной лаборатории, могут несколько изменяться. Поэтому в бланке результатов исследования в каждом медицинском учреждении обязательно указываются значения нормы, которые приняты в нем. На них будет ориентироваться врач при расшифровке анализа. Электрофорез белков крови назначают не очень часто, так как сегодня современные лабораторные исследования позволяют провести анализ на определенный белок, что ускоряет процесс диагностики. Абсолютным показанием к электрофорезу является наличие монолокальной гаммапатии. Также иногда анализ может быть показан в таких случаях:
При общей диспансеризации и получении медицинских справок для трудоустройства данное исследование крови не осуществляется. Не требуется оно и в процессе подготовки человека к хирургическому вмешательству. Для получения наиболее точных результатов рекомендуется соблюдение правил подготовки к анализу. Они включают в себя голодную диету в течение 15 часов до того как будет взята кровь, когда пациент может употреблять только чистую не газированную воду. За 90 минут до проведения исследования необходимо полностью исключить нагрузки как эмоциональные, так и физические, и курение в активной или пассивной форме. Чтобы не допустить искажение данных, забор материала не проводят сразу после того, как был осуществлен гемодиализ или проведена процедура, при которой использовались радиоконтрастные составы. Важно также, чтобы за несколько дней до исследования полностью было исключено лечение пенициллином, так как он вызывает расщепление амбулина, что исказит результат.
Исказить показатели, кроме неправильной подготовки к проведению анализа, могут 2 фактора: недавно проведенная процедура гемодиализа, из-за которой произошло разрушение эритроцитов в крови, и повышенный уровень билирубина в организме. В любом из этих случаев потребуется пересдача анализа через некоторое время, которое определит врач. источник ПРИНЦИП МЕТОДА: Метод основан на различии величины заряда белков сыворотки крови. Если нанести каплю сыворотки на полоску хроматографической бумаги, смоченной буферным раствором, и пропустить через эту полоску постоянный электрический ток, отдельные белки будут продвигаться в электрическом поле с различной скоростью. При рН=8,6 белки сыворотки крови движутся по направлению к аноду, поскольку они обладают в этих условиях отрицательным зарядом. Наиболее быстро движутся альбумины, затем 1- и 2-глобулины, далее — глобулины и наконец — глобулины. АППАРАТУРА: Прибор для определения белков в крови методом электрофореза на бумаге состоит из выпрямителя, электрофоретической кюветы и денситометра. Кюветы заполняются вероналовым буфером рН = 8,6. Нарезают из хроматографической бумаги полоски длиной 38 см., шириной 3 см., полоски смачивают буферным раствором и помещают в кювету. Ближе к отрицательному полюсу наносится сыворотка (0,01 мл), затем прибор включается в электрическую сеть. Электрофоретическое разделение белков сыворотки на бумаге производится обычно в течение 6- 24 часов при напряжении 150 Вт и силе тока 6-8 А. По истечении указанного срока бумажные полоски сушат в сушильном шкафу при температуре около 100 градусов в течение 5 мин., затем красят бромфеноловым синим. Остатки красителя, не связавшегося с белками, отмывают с полоски бумаги 10% уксусной кислотой. Количественное определение белковых фракций проводится с помощью денситометра или путём экстрагирования спиртовым раствором щелочи с последующим определением концентрация краски фотоколориметрически. Минеральный состав крови чрезвычайно разнообразен и играет большую роль в жизнедеятельности организма, например, в процессе роста и развития ребенка обмен кальция и связанных с ним фосфатов. Снижение содержания кальция может сопровождаться повышением нервно-мышечной возбудимости, судорогами (тетания новорожденных). Развитию гипокальциемии у новорожденных способствует сахарный диабет у матери, недоношенность и т.д. Чрезмерные дозы витамина «Д» вызывают гиперкальциемию с отрицательными последствиями для организма. Основным белком, осуществляющим снабжение тканей кислородом и освобождение их от углекислоты, является гемоглобин. В связи с этим, изучение обмена гемоглобина и определение его концентрации является чрезвычайно важным, а также актуальным является клиническое значение определения содержания желчных пигментов крови, моче и кале в дифференциальной диагностике различных видов желтух (гемолитическая, желтуха новорожденных, обтурационная, паренхиматозная). Минеральные составные части крови, значение их для организма. Различают несколько фракций кальция: ионизированный кальций, кальций неионизированный, но способный к диализу, и недиализирующийся (недиффундирующий), связанный с белками кальций. Кальций принимает активное участие в процессах нервно-мышечной возбудимости (как антагонист ионов К + ), мышечного сокращения, свертывания крови, образует структурную основу костного скелета, влияет на проницаемость клеточных мембран и т.д. Отчетливое повышение уровня кальция в плазме крови наблюдается при развитии опухолей в костях, гиперплазии или аденоме паращитовидных желез. В таких случаях кальций поступает в плазму из костей, которые становятся ломкими. Важное диагностическое значение имеет определение уровня кальция при гипокальциемии. Состояние гипокальциемии наблюдается при гипопаратиреозе. Нарушение функции паращитовидных желе приводит к резкому снижению содержания ионизированного кальция в крови, что может сопровождаться судорожными приступами (тетания). Понижение концентрации кальция в плазме отмечают также при рахите, спру, обтурационной желтухе, нефрозах и гломерулонефритах. Механизм свертывания крови. Система свертывания крови представляет собой каскадную цепь протеолитических реакций. Каскадность реакций обеспечивает постепенное усиление первоначального слабого сигнала – воздействия, вызывающего активацию внутреннего и внешнего пусковых механизмов свертывания. Каждая последующая стадия приводит к образованию все больших количеств активной формы очередного фактора. Происходит лавинообразное нарастание «мощности» каждой следующей ступени каскада, в результате стадия превращения фибриногена в фибрин протекает очень быстро. Первая стадия – сокращение поврежденного сосуда. Вторая стадия – образование белого тромба. Протромбин (VII фактор) под действием тромбопластина (III) тромбоцитов и ионов кальция (IV) превращается в активную форму – тромбин. В этой стадии участвуют факторы внешнего пускового механизма свертывания: проконвертин (VII); проакцелерин (V); фактор Стюарта (Х), а также факторы внутреннего пускового механизма свертывания: фактор Кристмаса (IХ); фактор Розенталя (ХI); фактор Хагемана (ХII) Третья стадия – образование красного тромба. Тромбин активирует фибриноген (I), превращая его в активную форму фибрин – мономер. Затем образуется фибрин – полимер (фибриновый гель), который не отличается прочностью. Его легко может разрушить механическое воздействие. Под действием фермента трансглутаминазы (ХIIIa) образуются прочные ковалентные связи между мономерами фибрина, а также между фибрином и белком фибронектином, стабилизируя гель фибрина. Через час тромб сжимается (ретракция тромба). Затем происходит фибринолиз (четвертая стадия). Плазминоген под действием фермента урокиназы и тканевого активатора плазминогена (ТАП) превращается в активную форму – плазмин (частичный протеолиз), который расщепляет в фибрине – полимере пептидные связи. Тромб в течение нескольких дней рассасывается. Роль витамина К в свертывании крови. Витамин К входит в состав ферментов, катализирующих карбоксилирование глутаминовой кислоты с образованием γ-карбоксиглутаминовой кислоты, входящей в состав факторов свертывания крови: II, VII, IХ, Х. Ингибиторы факторов свертывания крови: белок плазмы антитромбин III, инактивирующий большинство факторов свертывания крови; другие белки – ингибиторы протеиназ (α- макроглобулин, антиконвертин, тромбомодулин). гепарин, активирующий антитромбин III; антивитамины К – дикумарин, неодикумарин и др. Метаболизм гемоглобина. Синтез гема, гемоглобина. источник Определение количественных и качественных изменений основных фракций белка крови, используемое для диагностики и контроля лечения острых и хронических воспалений инфекционного и неинфекционного генеза, а также онкологических (моноклональных гаммапатий) и некоторых других заболеваний. Синонимы английские Serum Protein Electrophoresis (SPE, SPEP). Электрофорез на пластинках с агарозным гелем. Г/л (грамм на литр), % (процент). Какой биоматериал можно использовать для исследования? Как правильно подготовиться к исследованию?
Общая информация об исследовании Общий белок сыворотки крови включает в себя альбумин и глобулины, которые в норме находятся в определенном качественном и количественном соотношении. Оно может быть оценено с помощью нескольких лабораторных методов. Электрофорез белков в агарозном геле – это метод разделения белковых молекул, основанный на различной скорости их движения в электрическом поле в зависимости от размера, заряда и формы. При разделении общего белка сыворотки крови удается выявить 5 основных фракций. При проведении электрофореза белковые фракции определяются в виде полос различной ширины с характерным, специфичным для каждого типа белка местоположением в геле. Для определения доли каждой фракции в общем количестве белка оценивают интенсивность полос. Так, например, основная белковая фракция сыворотки – это альбумин. На его долю приходится около 2/3 всего белка крови. Альбумин соответствует самой интенсивной полосе, полученной при электрофорезе белков сыворотки крови здорового человека. К другим фракциям сыворотки, выявляемым с помощью метода электрофореза, относят: альфа-1 (преимущественно альфа-1-антитрипсин), альфа-2 (альфа-2-макроглобулин и гаптоглобин), бета (трансферрин и С3-компонент комплемента) и гамма-глобулины (иммуноглобулины). Различные острые и хронические воспалительные процессы и опухолевые заболевания сопровождаются изменением нормального соотношения белковых фракций. Отсутствие какой-либо полосы может указывать на дефицит белка, что наблюдается при иммунодефицитах или недостаточности альфа-1-антитрипсина. Избыток какого-либо белка сопровождается увеличением интенсивности соответствующей полосы, что наиболее часто наблюдается при различных гаммапатиях. Результат электрофоретического разделения белков может быть представлен графически, при этом каждая фракция характеризуется определенной высотой, отражающей ее долю в общем белке сыворотки. Патологическое увеличение доли какой-либо фракции носит название «пик», например «М-пик» при множественной миеломе. Исследование белковых фракций играет особую роль при диагностике моноклональных гаммапатий. В эту группу заболеваний входят множественная миелома, моноклональная гаммапатия неясного генеза, макроглобулинемия Вальденстрема и некоторые другие состояния. Эти заболевания характеризуются клональной пролиферацией В-лимфоцитов или плазматических клеток, при которой происходит бесконтрольная выработка одного вида (одного идиотипа) иммуноглобулинов. При разделении сывороточного белка пациентов с моноклональной гаммапатией с помощью электрофореза наблюдаются характерные изменения – появление узкой интенсивной полосы в зоне гамма-глобулинов, которая называется М-пик, или М-белок. М-пик может отражать гиперпродукцию любого иммуноглобулина (как IgG при множественной миеломе, так и IgM при макроглобулинемии Вальденстрема и IgA при моноклональной гаммапатии неясного генеза). Важно отметить, что метод электрофореза в агарозном геле не позволяет дифференцировать различные классы иммуноглобулинов между собой. Для этой цели используют иммуноэлектрофорез. Кроме того, данное исследование позволяет дать приблизительную оценку количества патологического иммуноглобулина. В связи с этим исследование не показано для дифференциальной диагностики множественной миеломы и моноклональной гаммапатии неясного генеза, так как она требует более точного измерения количества М-белка. С другой стороны, если диагноз «множественная миелома» был верифицирован, метод электрофореза в агарозном геле может быть использован для оценки динамики М-белка при контроле лечения. Следует отметить, что у 10 % пациентов с множественной миеломой нет никаких отклонений в протеинограмме. Таким образом, нормальная протеинограмма, полученная с помощью электрофореза в агарозном геле, не позволяет полностью исключить это заболевание. Другим примером гаммапатии, выявляемой с помощью электрофореза, является ее поликлональная разновидность. Она характеризуется гиперпродукцией различных видов (различных идиотипов) иммуноглобулинов, что определяется как однородное увеличение интенсивности полосы гамма-глобулинов при отсутствии каких-либо пиков. Поликлональная гаммапатия наблюдается при многих хронических воспалительных заболеваниях (инфекционных и аутоиммунных), а также при патологии печени (вирусных гепатитах). Исследование белковых фракций сыворотки крови используют для диагностики различных синдромов иммунодефицита. Примером может послужить агаммаглобулинемия Брутона, при которой снижается концентрация всех классов иммуноглобулинов. Электрофорез белков сыворотки пациента с болезнью Брутона характеризуется отсутствием или крайне низкой интенсивностью полосы гамма-глобулинов. Низкая интенсивность альфа-1-полосы – характерный диагностический признак недостаточности альфа-1-антитрипсина. Широкий спектр состояний, при которых наблюдаются качественные и количественные изменения протеинограммы, включает самые разные заболевания (от хронической сердечной недостаточности до вирусных гепатитов). Несмотря на наличие некоторых типичных отклонений протеинограммы, позволяющих в ряде случаев с определенной уверенностью диагностировать заболевание, обычно результат электрофореза белков сыворотки не может служить однозначным критерием постановки диагноза. Поэтому интерпретацию исследования белковых фракций крови проводят с учетом дополнительных клинических, лабораторных и инструментальных данных. Для чего используется исследование?
Когда назначается исследование?
источник
|