Для дошкольников и учеников 1-11 классов
Рекордно низкий оргвзнос 25 Р.
Описание презентации по отдельным слайдам:
Электрокинетические свойства дисперсных систем Подготовил: студент 213 группы Афлатунов Руфат
Электрокинетические явления Электрокинетические явления были открыты профессором Московского университета Ф.Ф.Рейсом в 1808 г. Электроосмос — явление переме-щения жидкой дисперсионной среды относительно неподвижной дисперсной фазы под действием электрического поля. Электрофорез — явление переме-щения дисперсной фазы относительно неподвижной жидкой дисперсионной среды под действием электрического поля
Потенциал течения (Квинке, 1859г) – возникновение разности потенциалов при движении дисперсионной среды относительно неподвижной дисперсной фазы. Потенциал оседания (Дорн, 1879) – возникновение разности потенциалов при движении дисперсной фазы относительно неподвижной дисперсионной среды. Открытые явления были названы электрокинетическими, так как в них обнаруживалась связь между скоростью протекания (кинетикой) и электрическим полем. Причиной электрокинетических явлений является наличие на границе раздела фаз двойного электрического слоя (ДЭС)
Причины возникновения ДЭС I. Неравенство электрохимических потенциалов ионов в кристаллической решетке тв. тела и ионов в растворе: Электрохимический потенциал – химический потен-циал плюс электрохимическая составляющая А. Адсорбционный механизм образования ДЭС Если , то иодид – ионы (потенциалопределяющие ионы – ПОИ) будут терять свою сольватную оболочку и адсорбироваться на поверхности твердой фазы, заряжая частицу отрицательно. К отрицательно заряженной частице из раствора за счет электростатического притяжения будут притягиваться ионы противоположного знака (противоионы – ПИ) — ионы калия.
В. Механизм поверхностной диссоциации Если , то иодид – ионы с поверхности будут переходить в раствор за счет поверхностной диссоциации и образовывать у поверхности внешнюю обкладку ДЭС. Поверхность твердой фазы в этом случае зарядится положительно — внутренняя обкладка ДЭС. II. Образование ДЭС за счет специфической адсорбции ионов, не входящих в кристаллическую решетка твердой фазы. Например, золь парафина в растворе гидроксида натрия. ПОИ – OH–, ПИ – Na+.
III. Образование ДЭС за счет ориентированной адсорбции ПАВ Соли жирных кислот в растворе диссоциируют, например натриевая соль стеариновой кислоты: — поверхностно–активный анион IV. Образование ДЭС за счет внешней разности потенциалов
Строение коллоидных мицелл Мицелла (Дюкло 1908г.) – частица дисперсной фазы вместе с ДЭС. Внутреннюю часть мицеллы составляет агрегат, состоящий из большого числа молекул или атомов малорастворимого соединения. Агрегат электронейтрален, но обладает большой адсорбционной способностью и способен адсорбировать на своей поверхности ионы из раствора – ПОИ. При выборе ПОИ пользуются правилом Фаянса-Панета-Пескова: «На твердой поверхности агрегата в первую очередь адсорбируются ионы, которые: входят в состав агрегата; способны достраивать кристаллическую решетку агрегата; образуют малорастворимое соединение с ионами агрегата; изоморфны с ионами агрегата.»
* Теория строения ДЭС Гельмгольца – Перрена (1879г) ДЭС – плоский конденсатор: внутренняя обкладка состоит из ПОИ, прочно связанных с поверхностью твердой фазы, а внешняя обкладка расположена в жидкости параллельно поверхности на расстоянии межмолекулярного порядка от нее. Поверхностный заряд (потенциал) – уменьшается линейно с расстоянием от поверхности в соответствии с теорией плоского конденсатора. Значение плотности поверхностного заряда (ρS , Кл/м2) — количество ПОИ на единицу площади поверхности рассчитывается в соответствии с теорией плоского конденсатора: где: ε — диэлектрическая проницаемость среды, ε0 — электрическая константа, равная 8,85·10-12 Ф/В, φ0 — разность потенциалов между дисперсной фазой и раствором, δ — расстояние между обкладками конденсатора, равное радиусу противоиона.
Теория строения ДЭС Гуи – Чепмена (1910-1913 гг.) Основные положения 1. ПИ вблизи заряженной стенки находятся под действием двух сил: электростатических и сил теплового движения, то есть на некотором расстоянии от поверхности. 2. ПИ рассматриваются как материальные точки, имеющие заряд, но не имеющие объема. 3. Распределение ПИ в поле электростатических сил поверхности твердой фазы подчиняется закону Больцмана: где: C0 = C+ + C– – концентрация ПИ и коионов в объеме раствора при φ = 0; Fzφ – работа по переносу 1 моль ионов из объема раствора, где φ = 0 в данную точку ДЭС (ПОИ заряжены отрицательно).
4. По мере удаления ПИ от поверхности, кулоновские силы ослабевают, а силы теплового движения возрастают. Это приводит к тому, что концентрация ПИ уменьшается и становится равной концентрации ионов в глубине раствора, возникает диффузный слой ПИ. 5. Дисперсионная среда непрерывна и характеризуется величиной диэлектрической проницаемости ε.
* В 1924 г. Штерн предложил схему строения ДЭС, в которой объединил теории Гельмгольца – Перрена и Гуи – Чепмена. По теории Штерна ПИ ориентируются около заряженной поверхности под действием трех сил: 1) электростатических (кулоновских) сил притяжения, 2) специфических (адсорбционных) сил притяжения; 3) сил теплового движения, стремящихся равномерно распределить ионы по объему ДЭС. Современные представления о строении ДЭС Теория Штерна
* Влияние электролитов на ДЭС Влияние индифферентных электролитов Индифферентный электролит – электролит, ионы которого не могут достраивать кристаллическую решетку агрегата. Пример: Формула мицеллы:
* Влияние неиндифферентных электролитов Неидифферентный электролит – электролит, ионы которого способны достраивать кристаллическую решетку дисперсной фазы, изменяя φ0. Пример: Формула мицеллы: 1. Добавим электролит, содержащий ион, способный достраивать кристаллическую решетку твердой фазы (одноименный с ПОИ) в данном случае добавим KJ. В этом случае: а) Иодид – ион J– будет достраивать кристаллическую решетку агрегата, тем самым увеличивая φ0 (кривая 2). б) Ион калия К+ будет увеличивать концентрацию ПИ, тем самым сжимая ДЭС (кривая 3).
* Измерение электрокинетического потенциала из явлений электрофореза и электроосмоса Электрокинетический потенциал – потенциал, возникающий на границе скольжения фаз при их относительном перемещении в электрическом поле. Электрокинетический потенциал отражает свойства ДЭС и определяется экспериментально из ЭКЯ. Скорость перемещения коллоидной частицы в электрическом поле зависит: напряженности внешнего электрического поля Н; от строения ДЭС коллоидной частицы – величины ζ; от свойств дисперсионной среды (вязкости η, диэлектрической проницаемости ε). Отношение линейной скорости перемещения частиц дисперсной фазы (дисперсионной среды) U, отнесенная к напряженности электрического поля Н, называется электрофоретической (электроосмотической) подвижностью U0:
* Электрокинетический потенциал связан с электрофоретической подвижностью, уравнением Гельмгольца – Смолуховского: где: h – смещение границы золь — боковая жидкость за время электрофореза; t – время электрофореза. где: Е – приложенная разность потенциалов; l – расстояние между электродами. Уравнение Гельмгольца — Смолуховского для электрофореза:
* Электроосмос Для расчета дзета-потенциала при электроосмосе заменяют линейную скорость (U) движения частицы на объемную (v): где: S – площадь капилляров мембраны (диафрагмы). Согласно закону Ома, напряженность электрического поля равна: Электрическое сопротивление связано удельной электропроводностью: Тогда получим: Уравнение Гельмгольца – Смолуховского для расчета дзета- потенциала при электроосмосе:
* Электрофорез применяют для: очистки, разделения медицинских препаратов, пищевых продуктов; нанесения тонких слоев неметаллических покрытий; получения изоляционных пленок, изготовления прорезиненных тканей и т.д. Электроосмос применяют для: обезвоживания грунта при возведении гидротехнических сооружений (платин, дамб); при сушке торфа и дерева; сушке стен и фундаментов сырых зданий; добыче нефти и т.д. Потенциал оседания является причиной грозовых разрядов в атмосфере. Потенциал течения – основа многих биологический процессов: течение крови через капилляры кровеносной системы дает биопотенциал. Потенциал течения возникают при транспортировке жидкого топлива (при протекании нефти вместе с водой образуется огромный заряд, приводящий к взрывам). Практическое значение электрокинетических явлений
Чтобы скачать материал, введите свой E-mail, укажите, кто Вы, и нажмите кнопку
Нажимая кнопку, Вы соглашаетесь получать от нас E-mail-рассылку
Если скачивание материала не началось, нажмите еще раз «Скачать материал».
источник
Электрокинетические свойства коллоидных систем. Электрофорез, электроосмос. Строение коллидных частиц лиофобных золей, электрокинетический потенциал. Влияние электролитов на величину электрокинетического потенциала. Изоэлектрическое состояние. Устойчивость и коагуляция коллоидных систем. Коагуляция электролитами, правило Шульце-Гарди.
Согласно общепринятой мицеллярной теории строения коллоидных растворов, золь (коллоидный раствор) состоит из двух частей: мицелл и интермицеллярной жидкости.
Мицелла – это частица дисперсной фазы золя, окруженная двойным электрическим слоем.
Интермицеллярной (межмицеллярной) жидкостью называют дисперсионную среду, разделяющую мицеллы, в которой растворены электролиты, неэлектролиты и ПАВ, являющиеся стабилизаторами коллоидной системы.
Частицы дисперсной фазы лиофобных золей имеют сложную структуру, которая зависит от условий получения золей. Предположим, что золь иодида серебра AgI образуется в ходе химической реакции между AgNO3 и KI. При этом основу коллоидных частиц составят микрокристаллы труднорастворимого AgI, включающие в себя m молекул AgI (а точнее, m пар ионов Ag + и I — ). Эти микрокристаллы называют агрегатами. Если реакция протекает в присутствии избытка иодида калия, то на поверхности агрегата возникает отрицательно заряженный слой в результате избирательной адсорбции n ионов I — . Иодид-ионы являются потенциалобразующими ионами (сокращенно ПОИ). Агрегат вместе с потенциалобразующими ионами является частицей твердой фазы и его называют ядром.
Под действием электростатических сил к ядру притягивается n ионов противоположного знака – противоионов, компенсирующих заряд ядра. В данном случае эту роль выполняют ионы K + . Часть противоионов (n — x), наиболее близко расположенных к ядру, находится в слое жидкости, смачивающем поверхность твердого ядра. Эти ионы испытывают действие не только электростатических, но и ван-дер-ваальсовых сил ядра, поэтому прочно удерживаются около него и образуют так называемый адсорбционный слой противоионов. Ядро с адсорбционным слоем противоионов образует коллоидную частицу. Остальные x противоионов, слабее связанных с ядром (только электростатически), под влиянием теплового движения располагаются в жидкой фазе диффузно (размыто), почему и носят название диффузного слоя. Все это образование вместе и является мицеллой.
Мицеллы золей электронейтральны. Структуру мицеллы можно записать в виде формулы:
,
где m – число молекул, входящих в состав агрегата, n – число потенциалобразующих ионов, (n – x) – число противоионов, входящих в адсорбционный слой, x – число противоионов, образующих диффузный слой.
Числа m, n и x могут изменяться в широких пределах в зависимости от условий получения и очистки золя. Обычно m >> n. Ядро вместе с адсорбционным слоем противоионов образуют собственно коллоидную частицу, или гранулу. В отличие от электронейтральной мицеллы коллоидная частица имеет заряд, в данном случае — отрицательный (x ‑ ).
Граница между коллоидной частицей и диффузным слоем носит название поверхность скольжения. В формуле мицеллы этой границе соответствует фигурная скобка между адсорбционным и диффузным слоями (на рис. 1 — сплошная линия).
Рис. 1. Схема строения мицеллы золя иодида серебра
с отрицательно заряженными частицами.
Граница скольжения обозначает ту геометрическую поверхность, по которой происходит разделение («разрыв») мицеллы на коллоидную частицу и диффузный слой в случае ее перемещения относительно дисперсионной среды (например, при участии мицеллы в броуновском движении или при движении под действием электрического поля).
На границе раздела твердое тело – жидкость возникает двойной электрический слой. Согласно современным представлениям, двойной электрический слой (ДЭС) — это образующийся на границе двух фаз тонкий поверхностный слой из пространственно разделенных электрических зарядов противоположного знака (потенциалобразующих ионов и противоионов). Потенциалобразующие ионы, адсорбирующиеся на твердой поверхности, — это внутренняя обкладка ДЭС. Внешняя обкладка ДЭС (слой противоионов) состоит из двух частей: плотной и диффузной.
Образование двойного слоя ионов приводит к появлению определенных электрических потенциалов на границе раздела твердой и жидкой фаз. Ионы первого слоя (внутренней обкладки), фиксированные на твердой поверхности, придают этой поверхности свой знак заряда и создают на ней так называемый поверхностный или φ-потенциал. Знак φ-потенциала совпадает со знаком заряда потенциалобразующих ионов. Величина φ-потенциала пропорциональна числу зарядов этих ионов на поверхности частиц.
С точки зрения термодинамики, φ-потенциал равен работе переноса единичного (элементарного) заряда из бесконечно удаленной точки объема раствора на поверхность твердой фазы, т. е. представляет собой потенциал твердой поверхности. Прямых методов его измерения не имеется.
Второй потенциал, характеризующий двойной слой ионов, называют электрокинетическим потенциалом или x-потенциалом (дзета-потенциалом). Он представляет собой электрический потенциал в двойном слое на границе между коллоидной частицей, способной к движению в электрическом поле и окружающей жидкостью. x-потенциал является потенциалом поверхности скольжения. Однако в двойном электрическом слое точное расстояние от твердой поверхности до поверхности скольжения неизвестно. Поэтому приближенно можно принять, что поверхность скольжения проходит по границе между адсорбционным и диффузным слоями противоионов. Следовательно x-потенциал близок, хотя и не совсем равен, потенциалу на границе адсорбционного и диффузионного слоев.
Термодинамически ξ-потенциал можно определить как работу, необходимую для переноса единичного заряда из бесконечно удаленного элемента объема раствора на поверхность скольжения. Знак ξ-потенциала обычно совпадает со знаком φ-потенциала. ξ-потенциал является частью φ‑потенциала и всегда меньше, чем φ‑потенциал. Величина ξ-потенциала непосредственно связана с числом противоионов в диффузном слое и изменяется пропорционально этому числу. Можно считать, что с увеличением толщины диффузного слоя ξ‑потенциал повышается. Поскольку электрокинетический потенциал относится к коллоидной частице и обусловливает ее подвижность в электрическом поле, величина этого потенциала может быть измерена экспериментально по скорости движения частиц. Направление же перемещения частиц к катоду или аноду указывает на знак ξ-потенциала.
Благодаря наличию ξ-потенциала на границах скольжения всех частиц дисперсной фазы возникают одноименные заряды и электростатические силы отталкивания противостоят процессам агрегации. Таким образом, ξ-потенциал является одним из основных факторов агрегативной устойчивости гидрофобных золей. Величина, а иногда и знаки φ- и ξ-потенциалов могут изменяться под влиянием внешних воздействий (электролитов, разведения, повышения температуры). Особенно чувствителен к этим факторам ξ-потенциал.
14.2.Электрокинетические свойства коллоидных систем: электрофорез, электроосмос.
К электрокинетическим явлениям относят эффекты, связанные либо с относительным движением двух фаз под действием постоянного электрического поля, либо с возникновением разности потенциалов при относительном смещении двух фаз, на границе между которыми существует двойной электрический слой.
Электрокинетические явления подразделяют на две группы: прямые и обратные. К прямым относят те электрокинетические явления, которые возникают под действием внешнего электрического поля (электрофорез и электроосмос). Обратными называют электрокинетические явления, в которых при механическом перемещении одной фазы относительно другой возникает электрический потенциал (потенциал протекания и потенциал седиментации).
Электрофорез и электроосмос были открыты Ф. Рейссом (1808). Он обнаружил, что если во влажную глину погрузить две стеклянные трубки, заполнить их водой и поместить в них электроды, то при пропускании постоянного тока происходит движение частичек глины к одному из электродов.
Это явление перемещения частиц дисперсной фазы в постоянном электрическом поле было названо электрофорезом.
В другом опыте средняя часть U-образной трубки, содержащей воду, была заполнена толченым кварцем, в каждое колено трубки помещен электрод и пропущен постоянный ток. Через некоторое время в колене, где находился отрицательный электрод, наблюдалось поднятие уровня воды, в другом — опускание. После выключения электрического тока уровни воды в коленах трубки уравнивались.
Это явление перемещения дисперсионной среды относительно неподвижной дисперсной фазы в постоянном электрическом поле названо электроосмосом.
Позже Квинке (1859) обнаружил явление, обратное электроосмосу, названное потенциалом протекания. Оно состоит в том, что при течении жидкости под давлением через пористую диафрагму возникает разность потенциалов. В качестве материала диафрагм были испытаны глина, песок, дерево, графит.
Явление, обратное электрофорезу, и названное потенциалом седиментации, было открыто Дорном (1878). При оседании частиц суспензии кварца под действием силы тяжести возникала разность потенциалов между уровнями разной высоты в сосуде.
Все электрокинетические явления основаны на наличии двойного электрического слоя на границе твердой и жидкой фаз.
Из описанных явлений электрофорез имеет наиболее широкое практическое применение. При электрофорезе происходит направленное перемещение частиц дисперсной фазы в электрическом поле постоянного тока к электроду, знак которого противоположен знаку заряда частиц. Подвижность частиц в электрическом поле обусловлена тем, что при наложении внешней разности потенциалов происходит разрыв двойного электрического слоя по границе скольжения и частица получает заряд, соответствующий ее ξ-потенциалу. Противоионы диффузного слоя перемещаются при этом к противоположному электроду. Очевидно, что скорость движения частиц дисперсной фазы пропорциональна величине их ξ‑потенциала. Наблюдая электрофоретическое движение частиц, можно определить знак и величину ξ‑потенциала коллоидной частицы.
Величина ξ‑потенциала связана со скоростью электрофореза заряженных частиц зависимостью, названной уравнением Гельмгольца – Смолуховского:
, (1)
где k — коэффициент, зависящий от формы частиц (для сферических частиц k = 6, для цилиндрических k = 4); η – вязкость среды; υ – линейная скорость перемещения частиц (или границы золя); ε – относительная диэлектрическая проницаемость среды; Е – напряженность поля (градиент потенциала).
Линейная скорость υ изменяется пропорционально напряженности поля Е, поэтому не может служить характеристикой частиц. В связи с этим введено понятие электрофоретической подвижности υэф., равной скорости движения частицы при единичном градиенте потенциала (Е = 1):
. (2)
Экспериментально найденные значения подвижностей часто оказываются меньше расчетных. Несовпадение этих величин объясняете в основном тем, что теория Гельмгольца — Смолуховского не учитывает два явления: релаксационный эффект и электрофоретическое торможение. Первый из этих эффектов вызывается нарушением симметрии диффузного слоя вокруг частиц. Второй эффект обусловлен добавочным трением электрической природы при движении частиц и противоионов в противоположные стороны.
Методы электрофореза имеют большое теоретическое и практическое значение. Знание величины ξ-потенциала позволяет судить об устойчивости коллоидного раствора, поскольку изменение его устойчивости, как правило, происходит пропоционально изменению электрокинетического потенциала.
Электроосмос, как и электрофорез, получил широкое применение. Механизм электроосмоса заключается в следующем. Нерастворимый материал мембраны при контакте с жидкостью (водой) диссоциирует с поверхности, отщепляя в жидкость те или другие ионы. Возникает двойной электрический слой, внутренняя обкладка которого входит в состав твердой фазы, а противоионы диффузно располагаются в жидкости. При включении постоянного электрического тока противоионы диффузного слоя перемещаются к электроду соответствующего знака. Так как ионы в воде всегда гидратированы, то при движении иона с ним увлекается определенный объем дисперсионнной среды за счет сил молекулярного трения (вязкости) между гидратной оболочкой иона и окружающей жидкостью. Очевидно, что чем больше толщина диффузного слоя и меньше площадь поперечного сечения капилляра или поры мембраны, тем сильнее проявляется электроосмотический перенос жидкости. Метод электроосмоса имеет большое практическое применение в процессах обезвоживания и сушки многих пористых материалов или весьма концентрированных коллоидных систем. Дли этой цели применяют, например, электрофильтр-прессы.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Только сон приблежает студента к концу лекции. А чужой храп его отдаляет. 8806 — 

источник
Электрический заряд может возникать на любой твердой поверхности, находящейся в контакте с жидкостью. Значение удельного заряда сравнительно небольшое: например, для глины на границе с водой оно составляет несколько десятков милликулонов, поэтому поверхность куска глины массой 1 кг, равная сотым долям квадратного метра, будет иметь ничтожно малый электрический заряд. Частицы глины общей массой 1 кг реализуют поверхность в миллионы раз большую, чем ее сплошной кусок, что приводит к резкому увеличению заряда поверхности. Появление значительного заряда поверхности является причиной возникновения особых электрокинетических явлений, характерных только для дисперсных систем.
Электрокинетическими называют такие явления, которые возникают при воздействии электрического поля на дисперсные системы и в результате перемещения частиц дисперсной фазы или дисперсионной среды. Несмотря на различие электрокинетических явлений все они связаны с наличием двойного электрического слоя и определяются ζ-потенциалом, который именно поэтому и называют электрокинетическим.
Внешнее электрическое поле вызывает такие электрокинетические явления дисперсных систем, как электрофорез и электроосмос.
Электрофорез — это перемещение под действием электрического поля частиц дисперсной фазы относительно дисперсионной среды. Схема электрофореза показана на рис. 6.11, где частица дисперсной фазы для наглядности дана в увеличенном масштабе. При наложении внешнего электрического поля частицы дисперсной фазы начинают двигаться к электроду, знак заряда которого противоположен знаку ζ-потенциала; направление движения частицы на рисунке показано стрелкой.
Движение частиц при электрофорезе обусловлено притяжением разноименных зарядов. Диффузный слой не препятствует взаимодействию разноименных зарядов. Противоионы в этом слое подвижны, распределяются неравномерно и не в состоянии экранировать действие внешнего электрического поля на частицы дисперсной фазы. Движение частиц происходит по границе скольжения.
В процессе электрофореза нарушается сферическая симметрия диффузного слоя противоионов, и он начинает двигаться в сторону, противоположную движению частиц. Противоположно направленный поток частиц диффузного слоя тормозит движение частиц. Этот эффект называют электрофоретическим торможением (короткая стрелка на рис. 6.11).
Рис. 6.11. Схема электрофореза:
При электрофорезе происходит движение частиц дисперсной фазы в направлении силовых линий электрического поля. Электрофорез используют для получения новых материалов, нанесения покрытий, очистки веществ от примесей и выделения продуктов. В медицине электрофорез применяют для введения лекарственных веществ. На кожу пациента накладывают тампон, смоченный раствором лекарственного препарата, а сверху — электроды, к которым приложен низкий, безопасный для организма потенциал. В ходе этой процедуры частички лекарственного препарата под действием электрического поля переходят в ткани организма человека.
Электроосмосом называют перемещение дисперсионной среды под действием внешнего электрического поля (рис. 6.12). Движение дисперсионной среды обусловлено притяжением разноименных зарядов. Оно происходит зачастую в капиллярах и в каналах пористых тел. Когда ζ-потенциал отрицательный, то положительно заряженные противоионы диффузного слоя притягиваются к отрицательному электроду. Противоионы увлекают за собой жидкость, составляющую дисперсионную среду. В результате этого происходит движение жидкости, причем перемещение жидкой дисперсионной среды относительно частиц дисперсной фазы, как и в случае электрофореза, происходит по границе скольжения.
Рис. 6.12. Схема электроосмоса
1 — дисперсная система; 2 — перегородка
Электроосмос используют, например, для обезвоживания древесины и других пористых материалов: строительных, грунта, продуктов питания, сырья для пищевой промышленности и др. Влажную массу помещают между электродами, а вода в зависимости от структуры ДЭС движется к одному из них и собирается в специальной емкости.
Для осуществления электрофореза или электроосмоса необходимо внешнее электрическое поле, т.е. движение частиц при электрофорезе или среды при электроосмосе является следствием воздействия этого поля.
Следует отметить, что явление электрофореза характерно главным образом для коллоидных растворов (золей), т.е. для систем, у которых размеры частиц дисперсной фазы не превышают 0,1 мкм. Электроосмос может наблюдаться не только в отношении коллоидных растворов, которые являются высокодисперсными системами, но и в отношении средне- и грубодисперсных систем.
источник
К электрокинетическим явлениям относят эффекты, связанные либо с относительным движением двух фаз под действием постоянного электрического поля, либо с возникновением разности потенциалов при относительном смещении двух фаз, на границе между которыми существует двойной электрический слой.
Электрокинетические явления подразделяют на две группы: прямые и обратные. К прямым относят те электрокинетические явления, которые возникают под действием внешнего электрического поля (электрофорез и электроосмос). Обратными называют электрокинетические явления, в которых при механическом перемещении одной фазы относительно другой возникает электрический потенциал (потенциал протекания и потенциал седиментации).
Электрофорез и электроосмос были открыты Ф. Рейссом (1808). Он обнаружил, что если во влажную глину погрузить две стеклянные трубки, заполнить их водой и поместить в них электроды, то при пропускании постоянного тока происходит движение частичек глины к одному из электродов.
Это явление перемещения частиц дисперсной фазы в постоянном электрическом поле было названо электрофорезом.
В другом опыте средняя часть U-образной трубки, содержащей воду, была заполнена толченым кварцем, в каждое колено трубки помещен электрод и пропущен постоянный ток. Через некоторое время в колене, где находился отрицательный электрод, наблюдалось поднятие уровня воды, в другом опускание. После выключения электрического тока уровни воды в коленах трубки уравнивались.
Это явление перемещения дисперсионной среды относительно неподвижной дисперсной фазы в постоянном электрическом поле названо электроосмосом.
Позже Квинке (1859) обнаружил явление, обратное электроосмосу, названное потенциалом протекания. Оно состоит в том, что при течении жидкости под давлением через пористую диафрагму возникает разность потенциалов. В качестве материала диафрагм были испытаны глина, песок, дерево, графит.
Явление, обратное электрофорезу, и названное потенциалом седиментации, было открыто Дорном (1878). При оседании частиц суспензии кварца под действием силы тяжести возникала разность потенциалов между уровнями разной высоты в сосуде.
Все электрокинетические явления основаны на наличии двойного электрического слоя на границе твердой и жидкой фаз.
Из описанных явлений электрофорез имеет наиболее широкое практическое применение. При электрофорезе происходит направленное перемещение частиц дисперсной фазы в электрическом поле постоянного тока к электроду, знак которого противоположен знаку заряда частиц. Подвижность частиц в электрическом поле обусловлена тем, что при наложении внешней разности потенциалов происходит разрыв двойного электрического слоя по границе скольжения и частица получает заряд, соответствующий ее ξ-потенциалу. Противоионы диффузного слоя перемещаются при этом к противоположному электроду. Очевидно, что скорость движения частиц дисперсной фазы пропорциональна величине их ξ‑потенциала. Наблюдая электрофоретическое движение частиц, можно определить знак и величину ξ‑потенциала коллоидной частицы.
Величина ξ‑потенциала связана со скоростью электрофореза заряженных частиц зависимостью, названной уравнением Гельмгольца – Смолуховского:
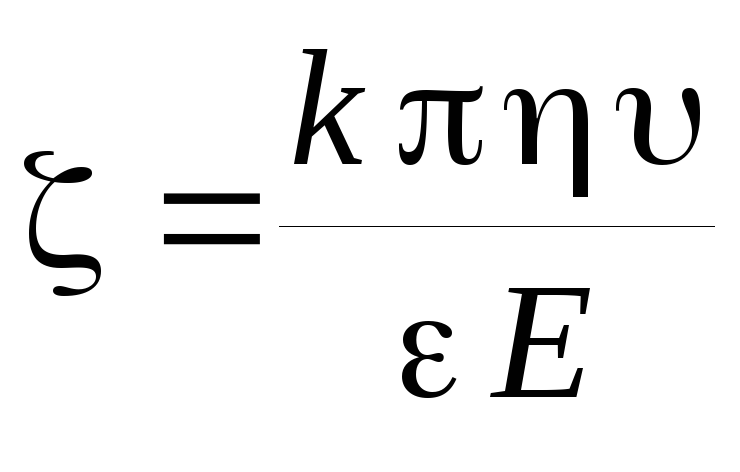
где k — коэффициент, зависящий от формы частиц (для сферических частиц k = 6, для цилиндрических k = 4); η – вязкость среды; υ – линейная скорость перемещения частиц (или границы золя); ε – относительная диэлектрическая проницаемость среды; Е – напряженность поля (градиент потенциала).
Линейная скорость υ изменяется пропорционально напряженности поля Е, поэтому не может служить характеристикой частиц. В связи с этим введено понятие электрофоретической подвижности υэф., равной скорости движения частицы при единичном градиенте потенциала (Е = 1):
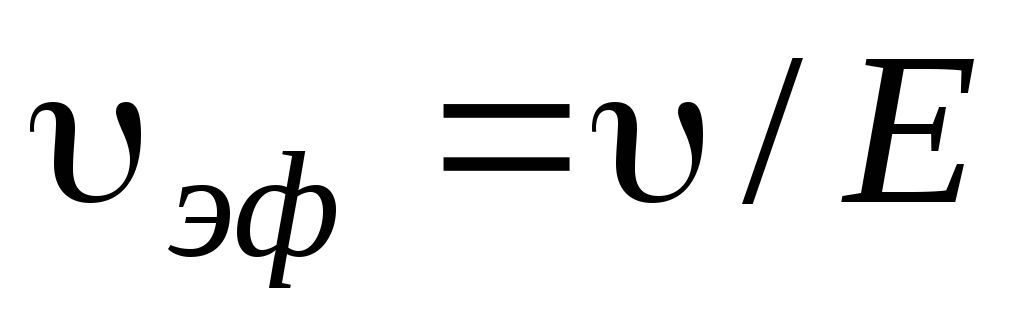
Экспериментально найденные значения подвижностей часто оказываются меньше расчетных. Несовпадение этих величин объясняете в основном тем, что теория Гельмгольца Смолуховского не учитывает два явления: релаксационный эффект и электрофоретическое торможение. Первый из этих эффектов вызывается нарушением симметрии диффузного слоя вокруг частиц. Второй эффект обусловлен добавочным трением электрической природы при движении частиц и противоионов в противоположные стороны.
Методы электрофореза имеют большое теоретическое и практическое значение. Знание величины ξ-потенциала позволяет судить об устойчивости коллоидного раствора, поскольку изменение его устойчивости, как правило, происходит пропоционально изменению электрокинетического потенциала.
Электроосмос, как и электрофорез, получил широкое применение. Механизм электроосмоса заключается в следующем. Нерастворимый материал мембраны при контакте с жидкостью (водой) диссоциирует с поверхности, отщепляя в жидкость те или другие ионы. Возникает двойной электрический слой, внутренняя обкладка которого входит в состав твердой фазы, а противоионы диффузно располагаются в жидкости. При включении постоянного электрического тока противоионы диффузного слоя перемещаются к электроду соответствующего знака. Так как ионы в воде всегда гидратированы, то при движении иона с ним увлекается определенный объем дисперсионнной среды за счет сил молекулярного трения (вязкости) между гидратной оболочкой иона и окружающей жидкостью. Очевидно, что чем больше толщина диффузного слоя и меньше площадь поперечного сечения капилляра или поры мембраны, тем сильнее проявляется электроосмотический перенос жидкости. Метод электроосмоса имеет большое практическое применение в процессах обезвоживания и сушки многих пористых материалов или весьма концентрированных коллоидных систем. Дли этой цели применяют, например, электрофильтр-прессы.
Виды устойчивости дисперсных систем. Лиофобные и лиофильные золи
Устойчивость дисперсных систем – это возможность их нахождения в исходном состоянии неопределенно долгое время.
Устойчивость дисперсных систем может быть:
К осаждению дисперсной фазы — характеризует способность дисперсной системы сохранять равновесное распределение фазы по объему дисперсионной среды или ее устойчивость к разделению фаз. Это свойство называется седиментационная (кинетическая) устойчивость.
Агрегативная устойчивость – это способность дисперсной системы сохранять неизменной во времени степень дисперсности, т.е. размеры частиц и их индивидуальность.
Она обусловлена способностью дисперсных систем образовывать агрегаты (т.е. укрупняться). По отношению к агрегации дисперсные системы могут быть устойчивыми кинетически и термодинамически. Термодинамически устойчивые системы образуются в результате самопроизвольного диспергирования одной из фаз, т.е. самопроизвольного образования гетерогенной свободнодисперсной системы. Дисперсные системы также делят на:
лиофильные, обладающие термодинамической устойчивостью;
лиофобные, которые термодинамически неустойчивы к агрегации, но могут быть устойчивы кинетически, т.е. обладать значительным временем жизни.
Особенности этих двух видов устойчивости показаны на схеме:
Термодинамическая устойчивость лиофильных систем означает, что они равновесны (энергия Гиббса G min), обратимы и образуются самопроизвольно, как из макрофаз, так и из истинных растворов. Поскольку образуются гетерогенные системы, то поверхностная энергия должна быть скомпенсирована энтропийной составляющей, т.е. частицы дисперсной системы должны участвовать в молекулярно кинетическом (тепловом) движении. Отсюда следует, что лиофильные системы могут быть только ультромикрогетерогенными, а поверхностное натяжение на границе «частица – среда» должно быть очень малым. Значение поверхностного натяжения, при котором обеспечивается термодинамическая устойчивость дисперсных систем, определяется соотношением Ребиндера – Щукина:
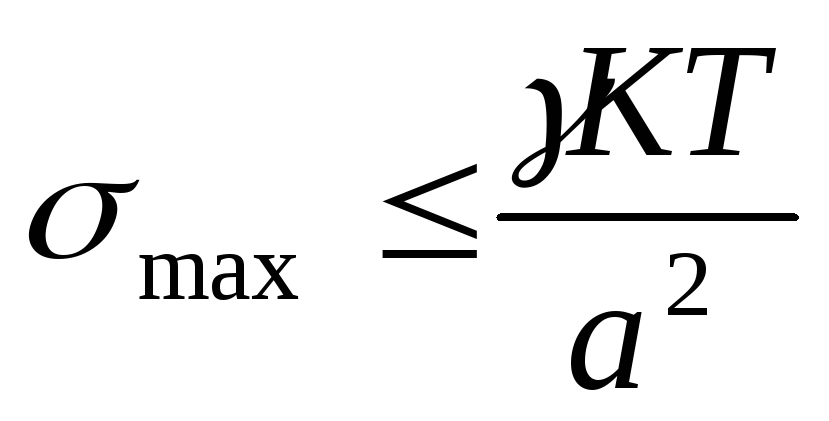
где ỵ езразмерный коэффициент;
а – средний размер частицы.
Расчеты показывают, что межфазное поверхностное натяжение в лиофильных дисперсных системах в зависимости от размеров частиц может иметь значение от 1,410 -7 до 1,410 -3 Дж/м 2 . Типичными представителями лиофильных дисперсных систем являются растворы коллоидных поверхностно активных веществ (ПАВ) (ассоциативные коллоиды) и растворы полимеров (молекулярные коллоиды).
Лиофобные системы термодинамически неустойчивы, т.к. частицы дисперсной фазы склонны к агрегации. Их агрегативная термодинамическая неустойчивость обусловлена избытком поверхностной энергии. Межфазное натяжение в них больше рассчитанного по соотношению Ребиндера – Щукина, поэтому они не могут быть получены самопроизвольным диспергированием. Для их образования должна быть затрачена внешняя энергия. Укрупнение частиц дисперсной фазы при потере агрегативной устойчивости достигается двумя путями:
Изотермическая перегонка, т.е. растворение мелких и рост крупных частиц в соответствии с уравнением Кельвина;
За счет слипания частиц, т.е. коагуляцией.
В зависимости от природы среды и концентрации дисперсной фазы эти процессы могут заканчиваться или осаждением, или структурообразованием.
При нарушении агрегативной устойчивости происходит коагуляция.
Правила коагуляции электролитами. Порог коагуляции. Правило Шульце-Гарди. Виды коагуляции: концентрационная и нейтрализационная. Коагуляция смесями электролитов. Явление «неправильные ряды». Механизм и кинетика коагуляции
Коагуляцией называется процесс слипания частиц с образованием крупных агрегатов. В результате коагуляции система теряет свою седиментационную устойчивость, так как частицы становятся слишком крупными и не могут участвовать в броуновском движении.
Коагуляция является самопроизвольным процессом, так как она приводит к уменьшению межфазной поверхности и, следовательно, к уменьшению свободной поверхностной энергии.
Различают две стадии коагуляции.
1 стадия – скрытая коагуляция. На этой стадии частицы укрупняются, но еще не теряют своей седиментационной устойчивости.
2 стадия — явная коагуляция. На этой стадии частицы теряют свою седиментационную устойчивость. Если плотность частиц больше плотности дисперсионной среды, образуется осадок.
Причины коагуляции многообразны. Едва ли существует какое либо внешнее воздействие, которое при достаточной интенсивности не вызывало бы коагуляцию.
источник
Что движется? Движется одна из фаз — или дисперсионная среда (жидкость) или дисперсная фаза(частицы). Электрокинетические явления – явления, связанные с существованием электрического заряда на границе раздела фаз и движением фаз относительно друг друга.
Почему движется? В одних случаях взаимное смещение фаз вызывается внешним электрическим полем (электроосмос и электрофорез); в других, напротив, относительное смещение фаз приводит к возникновению разности потенциалов (потенциал течения и потенциал осаждения, или седиментации).
В 1809 г. профессор Московского университета Ф.Ф. Рейс опубликовал статью, в которой описал открытые в 1807 г. явления электрофореза и электроосмоса.Он обнаружил, что при приложении разности потенциалов к U-образному электролизеру, нижняя часть которого заполнена перегородкой из толченого кварца, вода в колене у отрицательного электрода поднимается. Электроосмос — это явление переноса жидкой дисперсионной среды через неподвижную капиллярно-пористую перегородку под действием внешнего электрического поля. Это открытие было во многом случайном, так как целью экспериментов было исследование электролиза воды (точнее – «парадокса Никольсона»), осуществляемое с помощью нового по тому времени источника электричества – Вольтова столба (Вольт). А само явление электроосмоса несколько ранее наблюдал П.И. Страхов.
Предположив, что если вода при контакте с частицами кварца приобрела положительный заряд, то частицы могли приобрести отрицательный заряд, Рейсс поставил опыт, в котором под действием разности потенциалов двигались частицы глины в воде.Электрофорез — это явление переноса частиц дисперсной фазы под действием внешнего электрического поля.
В 1892 г. С. Линдер и Г. Пиктон вернулись к опытам Ф. Рейса и подробно исследовали явление электрофореза. Они установили, что частички твердой фазы в лиозолях несут электрический заряд, чем и объясняется их направленное движение. А.Тизелиус в 1937 применил электрофорез для анализа биополимеров, в частности методом электрофореза разделял сыворотку крови на пять белковых фракций.
Эффект, противоположный электроосмосу – возникновение потенциала течения обнаружил профессор Берлинского университета Георг Герман Квинке в 1859 г. Квинке было обнаружено, что при протекании жидкости через неподвижную пористую перегородку мембрану на расположенных по разные стороны от нее электродах возникает разность потенциалов.
И наконец, в 1878 году немецкий физик — экспериментатор Фридрих Эрнст Дорн обнаружил явление, обратное электрофорезу — потенциал оседания (потенциал седиментации), то есть возникновение разности потенциалов при оседании частиц суспензии кварца в воде обнаружил возникновение разности потенциалов — явление возникновения разности потенциалов в результате движения частиц дисперсной фазы относительно неподвижной дисперсионной среды.
Существование электрокинетических явлений связано со строением двойного электрического слоя и возникновением z-потенциала на границе раздела фаз.
Первую теорию электрокинетических явлений предложил Г. Гельмгольц, затем её развивали М. Смолуховский, Д. Генри и др. Уравнение, которое связывает скорость движения фаз друг относительно друга и электрокинетический потенциал называют уранением Гельмгольца-Смолуховского. Оно лежит в основе экспериментальных методов определения электрокинетического потенциала, потенциалов течения и оседания.
Для экспериментального исследования электрокинетических явлений были предложены различные приборы. В частности электрофорез можно наблюдать с помощью простейшего прибора Кёна, который представляет собой U-образную трубку с двумя кранами, имеющими отверстия, равные внутреннему диаметру трубки. Другие приборы для изучения электрофореза предложены Абрамсоном, Гиттрорфом и Тизелиусом. Прибор Думанского используется для определения знака заряда волокон. Электроосмотические методы определения электрокинетического потенциала основаны ни измерении объема перенесенной жидкости. Один из первых подобных приборов был предложен еще Ж.Б. Перреном
источник
Федеральное Агентство по образованию РФ
ШАХТИНСКИЙ ИНСТИТУТ (ФИЛИАЛ)
ТЕХНИЧЕСКОГО УНИВЕРСИТЕТА (НПИ)
на тему: «Электрофорез и электроосмос»
К защите Защита принята с оценкой «__»__________2008 г. ________________________
___________________ «__»____________ 2008 г.
В данном реферате рассматриваются общие сведения о дисперсных системах, электрокинетические явления в них, в частности электрофорез и электроосмос, основные понятия, формулы. Также практическое применение электрокинетических явлений в науке и технике.
1 Электрокинетические явления
2 Практическое применение электрокинетических явлений
Список используемых источников
Дисперсные системы. Кристаллы любого вещества, например сахара или хлорида натрия, можно получить разного размера – крупные и мелкие. Каков бы ни был размер кристаллов, все они имеют одинаковую для данного вещества внутреннюю структуру – молекулярную или ионную кристаллическую решетку.
При растворении в воде кристаллов сахара и хлорида натрия образуются соответственно молекулярные и ионные растворы. Таким образом, одно и то же вещество может находиться в различной степени раздробленности: макроскопически видимые частицы (>0,2 – 0,1 мм, разрешающая способность глаза), микроскопически видимые частицы (от 0,2 – 0,1мм до 400 – 300 нм*, разрешающая способность микроскопа при освещении белым светом) и в молекулярном (или ионном) состоянии. Постепенно складывались представления о том, что миром молекул и микроскопически видимых частиц находится область раздробленности вещества с комплексом новых свойств, присущих этой форме организации вещества.
Представим себе кубик какого-либо вещества, который будем разрезать параллельно одной из его плоскостей, затем полученные пластинки начнем нарезать на палочки, а последние на кубики. В результате такого диспергирования (дробления) вещества получаются плёночно-, волокнисто- и корпускулярнодисперсные (раздробленные) системы. Если толщина пленок, поперечник волокон или частиц (корпускул) меньше разрешающей способности оптического микроскопа, то они не могут быть обнаружены с его помощью. Такие невидимые в оптический микроскоп частицы называют коллоидными, а раздробленное (диспергированное) состояние веществ с размером частиц от 400 – 300 нм до 1 нм – коллоидным состоянием вещества.
1. Электрокинетические явления
Электрокинетическими явлениями называют перемещение одной фазы относительно другой в электрическом поле и возникновение разности потенциалов при течении жидкости через пористые материалы (потенциал протекания) или при оседании частиц (потенциал оседания). Перенос коллоидных частиц в электрическом поле называется электрофорезом, а течение жидкости через капиллярные системы под влиянием разности потенциалов – электроосмосом. Оба эти явления были открыты профессором Московского университета Ф. Ф. Рейссом в 1809 г.
Рейсс поставил два эксперимента. В одном из них он использовал U-образную трубку, перегороженную в нижней части диафрагмой из кварцевого песка и заполненную водой. При наложении электрического поля он обнаружил движение жидкости в сторону отрицательно заряженного электрода. Происходящее до тех пор, пока не устанавливалась определенная разность уровней жидкости (равновесие с гидростатическим давлением). Поскольку без диафрагмы движение жидкости отсутствовало, то последовал вывод о заряжении жидкости при контакте с частицами кварца. Явление получило название электроосмоса.
В другом эксперименте Ф. Ф. Рейсс погрузил в глину две стеклянные трубки, заполнил их водой и после наложения на них электрического поля наблюдал перемещение частиц глины в жидкости в направлении положительно заряженного электрода. Это был электрофорез. Таким образом, было обнаружено, что частицы имеют заряд, противоположный заряду жидкости.
Первые количественные исследования электроосмоса были выполнены Видеманном (1852). Он показал, что объёмная скорость υ электроосмоса пропорциональна силе тока I при прочих фиксированных параметрах, а отношение υ/I не зависит от площади сечения и толщены диаграммы.
В 1859 г. Квинке показал, что существует явление, обратное электроосмосу, т. е. при течении жидкости через пористое тело под влиянием перепада давлений возникает разность потенциалов. Возникновение разности потенциалов Квинке наблюдал при течении воды и водных растворов через разнообразные пористые материалы (глина, дерево, песок, графит и др.). Это явление получило название потенциала течения (или протекания). Позже было установлено, что потенциал течения не зависит от размера диаграммы, количества фильтруемой жидкости, но, как и при электроосмосе, пропорционален объёмной скорости фильтрации.
Количественное исследование эффекта, обратного электрофорезу, впервые было выполнено Дорном в 1878 г. Он измерял возникающую разность потенциалов при седиментации частиц суспензии кварца в центробежном поле. Явление возникновения разности потенциалов при осаждении дисперсной фазы получило название потенциала седиментации или оседания (или эффект Дорна).
Таким образом, по причинно-следственным признакам электрокинетические явления делят на две группы. К первой группе относят явления, при которых относительное движение фаз вызывается электрической разностью потенциалов, это электроосмос и электрофорез. Ко второй группе электрокинетических явлений принадлежат потенциал течения и потенциал седиментации, в которых возникновение электрической разности потенциалов обусловлено относительным движением фаз.
Наибольшее практическое применение получили электрофорез и электроосмос.
Основную роль в возникновении электрокинетических явлений играет двойной электрический слой (ДЭС), формирующийся у поверхности раздела фаз. Внешнее электрическое поле, направленное вдоль границы раздела фаз, вызывает смещение одного из ионных слоев, образующих ДЭС, по отношению к другому, что приводит к относительному перемещению фаз, т. е. к электроосмосу или электрофорезу. Аналогичным образом при относительном движении фаз, вызываемом механическими силами, происходит перемещение ионных слоев ДЭС, что приводит к пространственному разделению зарядов (поляризации) в направлении движения и к перепаду электрического потенциала (потенциал течения, потенциал оседания).
Направленное перемещение жидкости в пористом теле под действием приложенной разности потенциалов называется электроосмосом. Рассмотрим, например, электроосмотическое скольжение электролита в капилляре или порах мембраны. Примем для определенности, что на поверхности адсорбированы отрицательные ионы, которые закреплены неподвижно, а положительные ионы формируют диффузную часть ДЭС. Внешнее поле Е направлено вдоль поверхности. Электростатическая сила, действующая на любой произвольный элемент диффузной части ДЭС, вызывает движение этого элемента вдоль поверхности. Поскольку плотность заряда в диффузной части ДЭС Ф(х ) меняется в зависимости от расстояния до поверхности х (рис. 1), разложенные слои жидкого электролита движутся с разными скоростями. Стационарное состояние (неизменность во времени скорости течения) будет достигнуто, когда действующая на произвольный слой жидкости электростатическая сила скомпенсируется силами вязкого сопротивления, возникающими из-за различия скоростей движения слоев жидкости, находящихся на разном удалении от поверхности. Уравнения гидродинамики, описывающие движение жидкости при постоянных вязкости жидкости
источник
| Название: Электрокинетические явления в дисперсных системах Раздел: Рефераты по химии Тип: курсовая работа Добавлен 12:41:35 03 марта 2008 Похожие работы Просмотров: 1830 Комментариев: 15 Оценило: 3 человек Средний балл: 5 Оценка: неизвестно Скачать |
 будет определяться известной из физики формулой:
будет определяться известной из физики формулой: (I.1)
(I.1) ), который
), который , соответственно обозначить через С+ и С— , то для расстояния x=
, соответственно обозначить через С+ и С— , то для расстояния x= :
:
 Например, разрыв двойного слоя может произойти вследствие седиментации или броуновского движения частиц дисперсной фазы. Плоскость скольжения обычно проходит по диффузному слою, и часть его ионов остаётся в дисперсной среде. В результате дисперсионная среда и дисперсная фаза оказываются противоположно заряженными. Потенциал, возникающий на плоскости скольжения при отрыве части диффузного слоя, называется электрокинетическим потенциалом или
Например, разрыв двойного слоя может произойти вследствие седиментации или броуновского движения частиц дисперсной фазы. Плоскость скольжения обычно проходит по диффузному слою, и часть его ионов остаётся в дисперсной среде. В результате дисперсионная среда и дисперсная фаза оказываются противоположно заряженными. Потенциал, возникающий на плоскости скольжения при отрыве части диффузного слоя, называется электрокинетическим потенциалом или 


 . Из данного соотношения следует, что понижение температуры, введение в систему индифферентного электролита (специфически не взаимодействующего с поверхностью) и увеличение заряда его ионов ведут к уменьшению электрокинетического потенциала. Этот потенциал будет снижаться и с уменьшением диэлектрической проницаемости среды, например, при добавлении в водный раствор спиртов, эфиров и других органических веществ.
. Из данного соотношения следует, что понижение температуры, введение в систему индифферентного электролита (специфически не взаимодействующего с поверхностью) и увеличение заряда его ионов ведут к уменьшению электрокинетического потенциала. Этот потенциал будет снижаться и с уменьшением диэлектрической проницаемости среды, например, при добавлении в водный раствор спиртов, эфиров и других органических веществ. (III.1)
(III.1) и
и  (III.2)
(III.2)
 =
=  (III.3)
(III.3) =0, а
=0, а  и
и 
 (III.4)
(III.4) (III.5)
(III.5) (III.6)
(III.6) (III.7)
(III.7) -удельная электропроводность.
-удельная электропроводность. (III.8)
(III.8) будет разная. Ионы адсорбируются на стенках капилляра. Электропроводность будет больше в капилляре.
будет разная. Ионы адсорбируются на стенках капилляра. Электропроводность будет больше в капилляре. (III.9)
(III.9) -поверхностная проводимость (избыток электропроводности, связанный с наличием на стенках капилляра двойных электрических слоёв).
-поверхностная проводимость (избыток электропроводности, связанный с наличием на стенках капилляра двойных электрических слоёв). длина окружности капилляра.
длина окружности капилляра. (III.10)
(III.10) (III.11)
(III.11) и расчетное значение
и расчетное значение  р.
р. (IV.1)
(IV.1)
 (IV.2)
(IV.2) (IV.3)
(IV.3) (IV.4)
(IV.4)