Микроскопический анализ мокроты проводят как в нативных, так и в окрашенных препаратах. Препарат вначале просматривают при малом увеличении для первоначальной ориентировки и поиска крупных элементов (спирали Куршмана), а затем при большом увеличении для дифференцирования форменных элементов.
Спирали Куршмана (H.Curschmann, 1846-1910, немецкий врач) представляют собой беловато-прозрачные штопорообразно извитые трубчатые образования, сформировавшиеся из муцина в бронхиолах. Тяжи слизи состоят из центральной плотной осевой нити и спиралеобразно окутывающей её мантии, в которую бывают вкраплены лейкоциты (чаще эозинофилы) и кристаллы Шарко-Лейдена. Анализ мокроты, в котором обнаружены спирали Куршмана, характерен для спазма бронхов (чаще всего при бронхиальной астме, реже при пневмонии и раке лёгкого).
Кристаллы Шарко-Лейдена (J.M.Charcot, 1825-1893, французский невропатолог; E.V.Leyden, 1832-1910, немецкий невропатолог) выглядят как гладкие бесцветные кристаллы в форме октаэдров. Кристаллы Шарко-Лейдена состоят из белка, освобождающего при распаде эозинофилов, поэтому они встречаются в мокроте, содержащей много эозинофилов (аллергические процессы, бронхиальная астма).
Небольшое количество лейкоцитов можно обнаружить в любой мокроте, при воспалительных (и особенно нагноительных) процессах их количество возрастает.
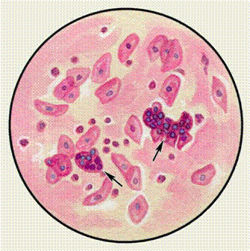
Нейтрофилы в мокроте. Обнаружение более 25 нейтрофилов в поле зрения свидетельствует об инфекции (пневмония, бронхит).
Эозинофилы в мокроте. Единичные эозинофилы могут встречаться в любой мокроте; в большом количестве (до 50-90% всех лейкоцитов) они обнаруживаются при бронхиальной астме, эозинофильных инфильтратах, глистных инвазиях лёгких и т.п.
Эритроциты в мокроте. Эритроциты появляются в мокроте при разрушении ткани лёгкого, пневмонии, застое в малом круге кровообращения, инфаркте лёгкого и т.д.
Плоский эпителий попадает в мокроту из полости рта и не имеет диагностического значения. Наличие в мокроте более 25 клеток плоского эпителия указывает на то, что данный образец мокроты загрязнён отделяемым из ротовой полости.
Цилиндрический мерцательный эпителий в небольшом количестве присутствует в любой мокроте, в большом — при поражении дыхательных путей (бронхит, бронхиальная астма).
Альвеолярные макрофаги локализуется в основном в межальвеолярных перегородках. Поэтому анализ мокроты, где присутствует хотя бы 1 макрофаг, указывает на то, что поражены нижние отделы дыхательной системы.
Эластические волока имеют вид тонких двухконтурных волоконец одинаковой на всё протяжении толщины, дихотомически ветвящихся. Эластичные волокна исходят из лёгочной паренхимы. Выявление в мокроте эластичных волокон свидетельствует о разрушении лёгочной паренхимы (туберкулёз, рак, абсцесс). Иногда их присутствие в мокроте используют для подтверждения диагноза абсцедирующей пневмонии.
Спирали Куршмана — Бронхоспастический синдром, наиболее вероятен диагноз астмы.
Кристаллы Шарко-Лейдена — Аллергические процессы, бронхиальная астма.
Эозинофилы, до 50-90% всех лейкоцитов — Аллергические процессы, бронхиальная астма, эозинофильные инфильтраты, глистная инвазия лёгких.
Нейтрофилы, более 25 в поле зрения — Инфекционный процесс. Судить о локализации воспалительного процесса невозможно.
Плоский эпителий, более 25 клеток в поле зрения — Примесь отделяемого из полости рта.
Альвеолярные макрофаги — Образец мокроты исходит из нижних дыхательных путей.
Эластические волокна — Деструкция лёгочной ткани, абсцедирующая пневмония.
Мокрота может содержать клетки злокачественных опухолей, особенно если опухоль растёт эндоброхиально или распадается. Определять клетки как опухолевые можно только в случае нахождения комплекса атипичных полиморфных клеток, особенно если они располагаются вместе с эластическими волокнами.
Мокрота в норме не содержит паразитов и яйца гельминтов. Выявление паразитов позволяет установить природу легочной инвазии, а также диагностировать кишечную инвазию и её стадию:
источник
Анализ мокроты расшифровка — это микроскопическое изучение клеток и их расшифровка. которая позволяет установить активность процесса при хронических болезнях бронхов и легких, диагностировать опухоли легкого.
Расшифровка анализа мокроты позволяют выявить различные заболевания.
Эозинофилы, составляют до 50-90% всех лейкоцитов, повышенные эозинофилы диагноструют заболевания:
- аллергические процессы;
- бронхиальная астма;
- эозинофильные инфильтраты;
- глистная инвазия лёгких.
Если количество нейтрофиов более 25 в поле зрения это говорит о наличии в организме инфекционного процесса.
Плоский эпителий, более 25 клеток в поле зрения — примесь отделяемого из полости рта.
Эластические волокна — Деструкция лёгочной ткани, абсцедирующая пневмония.
Спирали Куршмана диагностируют — бронхоспастический синдром, диагностика астмы.
Кристаллы Шарко-Лейдена диагностируют — аллергические процессы, бронхиальная астма.
Альвеолярные макрофаги — Образец мокроты идет из нижних дыхательных путей.
Мокрота выделяется при разнообразных заболеваниях органов дыхания. Анализ мокроты собирать ее лучше утром, перед этим надо прополоскать рот слабым раствором антисептика, затем кипяченой водой.
При осмотре отмечают суточное количество мокроты характер, цвет и запах мокроты, ее консистенцию, а также расслоение при стоянии в стеклянной посуде.
Анализы мокроты могут содержать:
- клеточные элементы крови,
- опухолевые клетки,
- простейшие микроорганизмы,
- личинки аскарид,
- растительные паразиты,
- различные бактерии и др.
| Показатель | Норма |
|---|---|
| Количество | 10-100 мл в сутки |
| Цвет | бесцветная |
| Запах | отсутствует |
| Слоистость | отсутствует |
| Реакция pH | нейтральная или щелочная |
| Характер | слизистая |
Повышенное выделение мокроты наблюдается при:
- отеке легких;
- абсцессе легких;
- бронхоэктатической болезни.
Если увеличение количества мокроты связано с нагноительным процессом в органах дыхания, это является признаком ухудшения состояния больного, если с улучшением дренирования полости, то расценивается как положительный симптом.
- гангрене легкого;
- туберкулезе легких, который сопровождается распадом ткани.
Пониженное выделение мокроты наблюдается при:
- остром бронхите;
- пневмонии;
- застойных явлениях в легких;
- приступе бронхиальной астмы (в начале приступа).
Зеленоватый
Зеленоватый цвет мокроты наблюдается при:
- абсцессе легкого;
- бронхоэктатической болезни;
- гайморите;
- посттуберкулезных нарушениях.
Различные оттенки красного
Отделение мокроты с примесью крови наблюдается при:
- туберкулезе;
- раке легкого;
- абсцессе легкого;
- отеке легких;
- сердечной астме.
Ржавый цвет мокроты наблюдается при:
- очаговой, крупозной и гриппозной пневмонии;
- туберкулезе легких;
- отеке легких;
- застойных явлениях в легких.
Иногда на цвет мокроты влияет прием некоторых лекарственных препаратов. При аллергии мокрота может быть ярко-оранжевого цвета.
Желто-зеленый или грязно-зеленый
Желто-зеленый или грязно-зеленый цвет мокроты наблюдается при различной патологии легких в сочетании с желтухой.
Черноватый или сероватый
Черноватый или сероватый цвет мокроты наблюдается у курящих людей (примесь угольной пыли).
Гнилостный запах мокроты наблюдается при:
- абсцессе легкого;
- гангрене легкого.
При вскрытии эхинококковой кисты мокрота приобретает своеобразный фруктовый запах.
- бронхите, осложненном гнилостной инфекцией;
- бронхоэктатической болезни;
- раке легкого, осложненном некрозом.
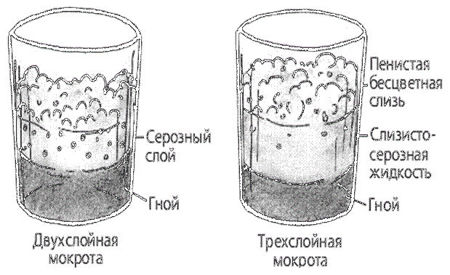
Двухслойная мокрота
Разделение гнойной мокроты на два слоя наблюдается при абсцессе легкого.
Трехслойная
Разделение гнилостной мокроты на три слоя – пенистый (верхний), серозный (средний) и гнойный (нижний) – наблюдается при гангрене легкого.
Кислую реакцию, как правило, приобретает разложившаяся мокрота.
Густая слизистая
Выделение густой слизистой мокроты наблюдается при:
- остром и хроническом бронхите;
- астматическом бронхите;
- трахеите.
Слизисто-гнойная
Выделение слизисто-гнойной мокроты наблюдается при:
- абсцессе легкого;
- гангрене легкого;
- гнойном бронхите;
- стафилококковой пневмонии;
- бронхопневмонии.
Выделение гнойной мокроты наблюдается при:
- бронхоэктазах;
- абсцессе легкого;
- стафилококковой пневмонии;
- актиномикозе легких;
- гангрене легких.
Серозная и серозно-гнойная
Выделение серозной и серозно-гнойной мокроты наблюдается при:
Кровянистая
Выделение кровянистой мокроты наблюдается при:
- раке легкого;
- травме легкого;
- инфаркте легкого;
- сифилисе;
- актиномикозе.
Альвеольные макрофаги
Большое количество альвеольных микрофагов в мокроте наблюдается при хронических патологических процессах в бронхолегочной системе.
Жировые макрофаги
Наличие в мокроте жировых макрофагов (ксантомных клеток) наблюдается при:
- абсцессе легкого;
- актиномикозе легкого;
- эхинококкозе легкого.
Клетки цилиндрического мерцательного эпителия
Наличие в мокроте клеток цилиндрического мерцательного эпителия наблюдается при:
Наличие в мокроте плоского эпителия наблюдается при попадании в мокроту слюны. Этот показатель не имеет диагностического значения.
- бронхите;
- бронхиальной астме;
- трахеите;
- онкологических болезнях.
Большое количество эозинофилов в мокроте наблюдается при:
- бронхиальной астме;
- поражении легких глистами;
- инфаркте легкого;
- эозинофильной пневмонии.
Эластические
Наличие эластических волокон в мокроте наблюдается при:
- распаде ткани легкого;
- туберкулезе;
- абсцессе легкого;
- эхинококкозе;
- раке легкого.
Наличие в мокроте обызвествленных эластических волокон наблюдается при туберкулезе легких.
Коралловидные
Наличие коралловидных волокон в мокроте наблюдается при кавернозном туберкулезе.
Спирали Куршмана
Наличие в мокроте спиралей Куршмана наблюдается при:
- бронхиальной астме;
- бронхите;
- опухоли легкого.
Кристаллы Шарко – Лейдена
Наличие в мокроте кристаллов Шарко -Лейдена – продуктов распада эозинофилов – наблюдается при:
- аллергии;
- бронхиальной астме;
- эозинофильных инфильтратах в легких;
- заражении легочной двуусткой.
Кристаллы холестерина
Наличие в мокроте кристаллов холестерина наблюдается при:
- абсцессе легкого;
- эхинококкозе легкого;
- новообразованиях в легких.
Кристаллы гематодина
Наличие в мокроте кристаллов гематодина наблюдается при:
- абсцессе легкого;
- гангрене легкого.
Бактериологический анализ мокроты необходим для уточнения диагноза выбора метода лечения, для определения чувствительности микрофлоры к различным лекарственным средствам, имеет большое значение для выявления микобактерии туберкулеза.
Появление кашля с мокротой требует обязательного обращения к врачу.
источник
Какие могут быть причины высокого уровня эозинофилов в крови или в тканях? Что это означает, от чего это зависит, и что делать в случае больших значений?
Термином эозинофилия обозначают состояние, при котором у пациента обнаруживаются повышенные уровни концентрации эозинофилов в крови.
Физиологические значения концентрации эозинофилов в периферической крови должны быть в пределах 350 млн. на литр крови.
О высоком уровне эозинофилов говорят, когда число клеток превышает 450 млн. на литр крови.
Эозинофилия может развиться независимо от возраста субъекта и не имеет никаких предпочтений (расы или пола). В развитых странах коррелирует с нарушениям аллергического характера, такими как астма или ринит, нетерпимость к еде. В развивающихся странах, вместо этого, обычно отмечается связь с заражением паразитами.
Не всегда эозинофилия тканей сопровождается эозинофилией крови или органов. Но, как правило, высокие значения эозинофилов в периферической крови являются признаком патологии или эозинофилического расстройства (если не удалось обнаружить какое-либо заболевание).
В зависимости от концентрации эозинофилов в крови, проводят следующую классификацию эозинофилии:
- Легкая эозинофилия. Когда число эозинофилов в периферической крови находится в пределах от 450 до 1500 млн. клеток на литр крови.
- Умеренная эозинофилия. Когда количество эозинофилов находится между 1500 и 5000 млн. клеток на литр крови.
- Тяжелая эозинофилия или гиперэозинофилия. Когда число эозинофилов превышает 5000 млн. клеток на литр крови.
Все эозинофилов принадлежат к клеткам крови и поэтому производятся в костном мозге, образуясь из стволовых кроветворных клеток.
Из костного мозга эозинофилы быстро переходят в кровь. Здесь число эозинофилов может увеличиться в силу трёх причин:
- Рост концентрации факторов, стимулирующих выработку эозинофилов. К указанной категории относятся интерлейкины IL-3 и IL-5 (белковые молекулы, которые могут изменять поведение других клеток), а также фактор гранулоцитов, известный под аббревиатурой GM-CSF.
- Потеря эффективности одного из факторов. Средняя продолжительность жизни эозинофилов составляет несколько часов (около 12), но действие некоторых факторов ингибирует цитокины, определяющие апоптоз (запрограммированную смерть), и, тем самым, определяют увеличение их концентрации в крови.
- Смесь двух предыдущих причин.
Причины, которые могут вызвать рассмотренные выше изменения, весьма разнообразны и разнородны, и будут рассмотрены далее в причинах, которые определяют эозинофилию.
Причины, которые могут увеличить концентрацию эозинофилов или продлить их срок жизни можно объединить следующим образом:
Идиопатическая или первичная эозинофилия. Увеличение популяции эозинофилов в крови в отсутствие основных патологий и причин, которые можно обнаружить.
Вторичная эозинофилия. Имеет место, когда эозинофилия связана с какой-либо другой патологией.
Распространенные заболевания, которые могут определить развитие эозинофилии:
- Аллергии, которые влияют на дыхательные пути. К этой категории принадлежат аллергический ринит или сенная лихорадка (воспаление слизистой оболочки носа) и астма (воспаление и обратимая обструкция нижних дыхательных путей).
- Кожные аллергии. Чрезмерная и ошибочная реакция иммунной системы на внешние раздражители, которые вступают в контакт с кожей. Пример патологии, принадлежащей к этой категории, и которая вызывает эозинофилию – это дерматит Дюринга или герпетиформный дерматит.
- Аллергия на лекарства. Симптомы, связанные с этим расстройством начинаются от простой сыпи и доходят до серьёзных проблем с дыханием, вплоть до анафилактического шока. Лекарства, которые чаще всего дают в таком случае: противоэпилептические, сульфаниламиды, нестероидные противовоспалительные средства.
- Непереносимость пищевых продуктов. Примером такой нетерпимости является гастроэнтерит, то есть нарушение работы желудка и первой части тонкого кишечника с диареей и проблемами с желудком, характеризуется инфильтрацией стенок желудка и кишечника от эозинофилов и увеличением их концентрации в периферической крови.
- Заражение паразитами. Наиболее распространенными у человека паразитами являются аскариды. Напомним, что аскариды – это черви, которые паразитируют в кишечнике и часто встречаются у жителей развивающихся стран.
- Грибковые инфекции. Примером может быть кандидоз. Это грибковая инфекция, которая может коснуться нескольких органов, причиной являются грибки Coccidioides immitis и Coccidioides posadasii.
- Лимфома Ходжкина. Новообразования в лимфоидной ткани, то есть в лимфоцитах.
- Неходжкинская лимфома. Злокачественные новообразования лимфатической ткани, которые первоначально возникают в лимфатических узлах.
- Некоторые крупные опухоли. Например, рак кишечника.
- Эозинофильный лейкоз. Группа заболеваний, характеризующихся аномальной пролиферацией клеток спинного мозга – предшественников эозинофилов. Симптоматики зависит от тканей, в которые эозинофилы проникают. Прогноз более негативный, в случае проникновения в ткани сердца.
- Интерстициальная нефропатия. Патология, которая приводит к повреждению канальцев междоузлий в почках, что, в свою очередь, приводит к острой почечной недостаточности.
- Аутоиммунные заболевания. Примером таких заболеваний является болезнь Крона и системная красная Волчанка.
- Некоторые формы васкулита. Все васкулиты являются воспалением кровеносных сосудов различной этиологии. Одна форма васкулита характеризуется повышенным уровнем эозинофилов, в частности синдром Черджа-Страусса. Васкулит, который влияет на мелкие кровеносные нескольких органов.
- Эмболия от холестерина. Обычно происходит во время операции по катетеризации. Введение катетера в сосуд может привести к отрыву атеросклеротических бляшек, которые способны привести к эмболии в других органах.
- Гипериммуноглобулиновый синдром. Системное заболевание, которое влияет на соединительную ткань и скелет.
Чтобы определить, имеет ли пациент проблемы с повышенным уровнем эозинофилом, следует, в первую очередь, провести анализ крови, то есть полную гемохромоцитометрию, т.е. подсчет полного числа клеток крови. И, вместе с этим, получение точного абсолютного числа эозинофилов.
При подтверждении высокой концентрации эозинофилов, переходят к поиску причины такого состояния. Для этого специалист, как правило, гематолог, выполняет протокол следующим образом:
- Анамнестический анализ. Предполагает изучение истории болезней пациента, в частности, поиск случаев паразитарной инфекции, возможной аллергии или непереносимости какого-либо пищевого продукта.
- Детальный осмотр.
- Гематохимический анализ – позволяет проверить функцию почек и печени.
- Мазок из носа и анализ образцов слизи, чтобы определить эозинофилию от аллергического ринита.
- Анализ мокроты, чтобы определить эозинофилию от аллергической астмы.
- Оценка осадка мочи для оценки наличия некоторых паразитов и аллергии на лекарства.
- Анализ кала, чтобы оценить возможность наличия глистов.
- Биопсия костного мозга для исследования возможных миелопролиферативных заболеваний.
- Экспертиза спинномозговой жидкости, чтобы определить наличие паразитов, среди которых могут быть как черви, так и грибки.
К этой серии исследований часто нужно добавить также ряд инструментальных обследований, чтобы оценить повреждения различных органов:
- Эхокардиограмма. Чтобы оценить влияние гиперэозинофилии на состояние сердца и образование тромбов.
- Компьютера томография. Для оценки поражения легких, мозга и брюшной полости, вызванных эозинофилией или исходной патологией.
- Цистоскопия. Используется для диагностики заражения шистосомами. Яйца шистосом, которые являются паразитами крови и определяют развитие эозинофилии, удаляются с мочой и, следовательно, из скопление может быть обнаружено во время цистоскопии.
Лечение вторичной эозинофилии предполагает лечение исходной патологии, которая должна быть исцелена, а если это невозможно, следует держать её под контролем.
Терапия идиопатической эозинофилии основывается на кортикостероидах. Сегодня для случаев серьёзной эозинофилии используется сочетание терапией кортизоном и интерфероном А.
Прогноз при эозинофилии, во многом, зависит от заболевания, вызывавшего изменение состояния крови.
источник
Прежде чем начать лечение респираторного заболевания, специалисты настаивают на подробной диагностике. В первую очередь, проводится микроскопия экссудата. По ее результатамидентифицируют эозинофилыв мокроте и другие компоненты. Они помогают уточнить тот или иной диагноз, обозначить восстановительный курс. Перед этим необходимо разобраться в особенностях подготовки, расшифровке данных и других значимых деталях.
Микроскопия мокроты – это значимое обследование, которое проводится среди пациентов, страдающих патологиями легочной системы или других органов данной структуры. Выведение экссудата идентифицируется во время кашлевых позывов, что представляет собой одно из показаний к началу диагностики. По ее результатам устанавливают локализацию и стадию воспаления.
Оттенок и консистенция секрета (вязкость, густота) свидетельствуют о конкретном заболевании. Учитывая полученные данные и конкретного возбудителя, пульмонолог назначит соответствующий курс восстановления. Важно помнить о том, что наличие или отсутствие патогенных микроорганизмов – это одно из главных доказательств недоброкачественных опухолей. Учитывая спектр возможностей микроскопии мокроты, отказываться от нее не следует.
Проводить посев необходимо пациентам, у которых имеет место подозрение на патологии респираторной системы – начальные или затяжные:
- любая стадия бронхита;
- опухоли, склонные к злокачественному перерождению;
- туберкулез легких;
- пневмония – воспалительные изменения в паренхиме.
Представленная категория лиц находится в группе риска. В связи с этим именно для них регулярные обследования экссудата представляют собой обязательную часть терапии. Проводится диагностика и после завершения восстановительного курса.
Чтобы эритроциты в мокроте и другие компоненты были идентифицированы правильно, необходимо должным образом «настроиться» на процедуру. Пульмонологи обращают внимание на то, что в человеческой ротовой полости сосредоточена особенная флора – именно она может смешиваться с патогенным секретом, нарушая итоги проверок.
В связи с этим перед микроскопией мокроты целесообразно:
- употреблять теплую воду в значительном количестве;
- использовать отхаркивающие лекарственные препараты;
- тщательно почистить зубы, воспользоваться зубной нитью и прополоскать рот перед диагностикой, используя специальные бальзамы.
Важно заранее отказаться от употребления алкоголя и курения, поскольку спирт и никотин также могут нарушить состав мокроты. Если не сделать этого за 12-16 часов до процедуры, в результатах ошибочно могут появиться эозинофилы или эритроциты.
Сбор экссудата осуществляется либо дома, либо в условиях амбулатории – в специально отведенных для этого комнатах. Человеку выдается стерильная баночка, которую откупоривают лишь перед сдачей «материала».
Правильнее всего собирать мокроту рано утром, потому что в это время она окажется наиболее свежей.
Секрет для микроскопии необходимо именно выкашливать. Его отхаркивание недопустимо, иногда в таких случаях ошибочно эластические волокна появляются в мокроте. В целях улучшения выведения мокроты пульмонологи настаивают на том, что нужно осуществить три медленных вдоха и выдоха. Между ними на пять минут задерживают дыхание.
Определить наличие или отсутствие эозинофилов в микроскопии мокроты позволят следующие рекомендации:
- Необходимо хорошенько прокашляться, а накопленную мокроту сплюнуть в емкость для анализа.
- Слюна, имеющаяся в ротовой полости, ни в коем случае не должна попадать в данную баночку.
- Повторяться подобные действия должны ровно до тех пор, пока соотношение мокроты не достигнет определенного уровня. Достаточной отметкой является пять мл.
Если по каким-либо причинам не получается добиться выведения мокроты, допустимо провести импровизированную ингаляцию. Например, подышать над кастрюлей с горячей водой. Это не должен быть кипяток, потому что он может обжечь слизистую поверхность носоглотки.
Сразу после сбора мокроты для микроскопии и выявления в ней эозинофилов, емкость закупоривают и отвозят в лабораторию. Экссудат должен быть свежим – не больше двух часов. Это связано с тем, что в нем могут быстро начать развиваться сапрофиты. Подобные микроорганизмы препятствуют корректной постановке диагноза. В связи с этим баночку с мокротой правильнее всего будет хранить в холодильнике, если такой возможности нет – в максимально холодном месте, но без застывания.
Присутствие эритроцитов в единичном количестве в микроскопии является нормой, это не оказывает какого-либо воздействия на итоги диагностики. Количество ежедневно вырабатываемой слизи в области трахеи и бронхов должно находиться границах от 10 до 100 мл. Если же эпителий попадает в мокроту, экссудат может изменяться по цвету и количеству.
Превышение представленной нормы является прямым свидетельством того, что понадобятся дополнительные проверки. Если какие-либо отклонения отсутствуют, то еще один анализ – мазок на МТБ – демонстрирует однозначный отрицательный результат.
На патологии указывают не только эозинофилы в микроскопии мокроты, но и другие составляющие.
| Компонент | Значение |
| Эпителий | Плоская разновидность не оказывает влияния на результаты проверки. Цилиндрическая является следствием астмы, бронхита или онкологического поражения легких |
| Альвеолярные макрофаги | Обнаружение возможно при частых и продолжительных контактах с пылью. Не менее вероятными диагнозами называют инфаркт легкого, митральный стеноз и даже застойные процессы в тканях системы |
| Лейкоциты | Несущественное количество может быть нормой. В то время как их присутствие в значительном соотношении указывает на онкологию, туберкулез, воспаление легких и коклюш |
| Эритроциты | Резкое возросшее количество является свидетельством кровотечения в респираторной системе. Чаще всего это происходит в легких |
| Эластичные волокна | С высокой долей вероятности являются предвестниками бронхиальной астмы, туберкулеза и пневмонии. Кристаллические образования Шарко-Лейдена (одна из разновидностей) идентифицируют при абсцессе, гангренозном поражении, а также раке или запущенном туберкулезе. |
Эозинофилы в результатах мокроты появляются при развитии астмы. Их опасность заключается в том, что абсолютное удаление из структуры дыхательных путей невозможно. Поэтому при первом появлении эозинофилов лечение рекомендуется проводить как можно быстрее.
Для уточнения диагноза проводятся дополнительные «прицельные» проверки, например, УЗИ, рентген, флюорография. Они позволяют идентифицировать конкретное заболевание, стадию его развития и поражение системы. Именно по итогам комплексной диагностики назначается восстановительный курс.
источник
Мокрота (sputum) — патологический секрет, образующийся при поражении трахеи, бронхиального дерева и легочной ткани. Ее выделение наблюдается не только при заболеваниях органов дыхания, но и сердечно-сосудистой системы. Общий анализ мокроты включает в себя макроскопическое, химическое, микроскопическое и бактериоскопическое определение ее свойств.
Увеличение количества мокроты может расцениваться как признак ухудшения состояния больного, если оно зависит от обострения, например нагноительного процесса; в других случаях, когда увеличение количества мокроты связано с улучшением дренирования полости, оно расценивается как положительный симптом. Уменьшение количества мокроты может являться следствием стихания воспалительного процесса или, в других случаях, результатом нарушения дренирования гнойной полости, часто сопровождаясь при этом ухудшением состояния больного.
Слизистая мокрота выделяется при острых бронхитах, хронических бронхитах, бронхиальной астме, при пневмониях, бронхоэктатической болезни, раке легкого. Слизисто-гнойная мокрота выделяется при хронических бронхитах, пневмониях, бронхоэктатической болезни, абсцессе легкого, при нагноившемся эхинококке легкого, актиномикозе легких, при раке легкого, сопровождающемся нагноением. Чисто гнойная мокрота обнаруживается при абсцессе легкого, нагноившемся эхинококке легкого, прорыве эмпиемы плевры в бронх, бронхоэктатической болезни.
Кровянистая мокрота, состоящая почти из чистой крови, наиболее часто отмечается при туберкулезе легких. Появление кровавой мокроты может быть при раке легкого, бронхоэктатической болезни, абсцессе легкого, при синдроме средней доли, инфаркте легкого, при травме легкого, актиномикозе и сифилисе. Кровохарканье и даже примесь крови к мокроте встречаются в 12—52% инфарктов легких. Примесь крови в мокроте определяется при опухолях легкого, при инфаркте легкого, при крупозной и очаговой пневмониях, силикозе легких, при застойных явлениях в легких, сердечной астме и отеке легких. Серозная мокрота выделяется при отеке легких.
Слизистая и серозная мокрота бесцветна или беловата. Присоединение гнойного компонента к мокроте придает ей зеленоватый оттенок, что характерно для абсцесса легкого, гангрены легкого, бронхоэктатической болезни, актиномикоза легкого.
Мокрота ржавого или коричневого цвета, указывает на содержание в ней не свежей крови, а продуктов ее распада (гематин) и встречается при крупозной пневмонии, при туберкулезе легких с творожистым распадом, застое крови в легких, отеке легких, при легочной форме сибирской язвы, инфаркте легкого.
Грязно-зеленый или желто-зеленый цвет может иметь мокрота, отделяющаяся при различных патологических процессах в легких, сочетающихся с наличием у больных желтухи. Желто-канареечный цвет имеет иногда мокрота при эозинофильных пневмониях. Мокрота цвета охры отмечается при сидерозе легкого. Черноватая или сероватая мокрота бывает при примеси угольной пыли. При отеке легких серозная мокрота, выделяющаяся нередко в большом количестве, бывает равномерно окрашенной в слабо-розовый цвет, что обусловлено примесью эритроцитов. Вид такой мокроты иногда сравнивают с жидким клюквенным морсом. Могут окрашивать мокроту некоторые лекарственные вещества. Так, например, антибиотик рифампицин окрашивает ее в красный цвет.
Гнилостный (трупный) запах мокрота приобретает при гангрене и абсцессе легкого, бронхоэктатической болезни, гнилостном бронхите, раке легкого, осложнившимся некрозом.
Примесь к мокроте только что принятой пищи отмечается при сообщении пищевода с трахеей или бронхом, что может возникать при раке пищевода.
При прорыве эхинококка легкого в бронх в мокроте могут быть обнаружены крючья или редко сколекс эхинококка. Очень редко в мокроте можно обнаружить зрелых аскарид, которые заползают в дыхательные пути у ослабленных больных, и личинок аскарид, попадающих в дыхательные пути при миграции их в легкие. Яйца легочной двуустки появляются в мокроте при разрыве кисты, образующейся в легком при паразитировании легочной двуустки. При гангрене и абсцессе легкого в мокроте могут обнаруживаться кусочки некротизированной ткани легкого. При опухоли легкого с мокротой иногда выделяются кусочки опухолевой ткани.
Фибринозные свертки, состоящие из слизи и фибрина, встречаются при фибринозном бронхите, при туберкулезе, пневмониях.
Рисовидные тельца (чечевицы) или линзы Коха состоят из детрита, эластических волокон и МБТ и встречаются в мокроте при туберкулезе.
Пробки Дитриха, состоящие из продуктов распада бактерий и легочной ткани, кристаллов жирных кислот, встречаются при гнилостном бронхите и гангрене легкого. При хронических тонзиллитах из миндалин могут выделяться пробки, напоминающие по внешнему виду пробки Дитриха. Пробки из миндалин могут выделяться и при отсутствии мокроты.
Свежевыделенная мокрота имеет щелочную или нейтральную реакцию. Разложившаяся мокрота приобретает кислую реакцию.
Определение белка в мокроте может явиться подспорьем при дифференциальной диагностике между хроническим бронхитом и туберкулезом: при хроническом бронхите в мокроте определяются следы белка, в то время как при туберкулезе легких в мокроте содержание белка больше, и он может быть определен количественно (до 100—120 г/л).
Желчные пигменты могут обнаруживаться в мокроте при заболеваниях дыхательных путей и легких, сочетающихся с желтухой, при сообщении между печенью и легким (при прорыве абсцесса печени в легкое). Помимо этих состояний, желчные пигменты могут быть обнаружены при пневмониях, что связано с внутрилегочным распадом эритроцитов и последующими превращениями гемоглобина.
Встречающиеся в мокроте клетки плоского эпителия диагностического значения не имеют. Клетки цилиндрического эпителия (как единичные, так и в виде скоплений) могут быть обнаружены при бронхиальной астме, бронхите, бронхогенном раке легкого. Вместе с тем появление клеток цилиндрического эпителия в мокроте может быть обусловлено и примесью слизи из носоглотки.
Альвеолярные макрофаги — клетки ретикулоэндотелия. Макрофаги, содержащие в протоплазме фагоцитированные частицы (так называемые пылевые клетки), встречаются в мокроте людей, находящихся в длительном контакте с пылью. Макрофаги, содержащие в протоплазме гемосидерин (продукт распада гемоглобина), называют «клетками сердечных пороков». «Клетки сердечных пороков» встречаются в мокроте при застое в легких, митральном стенозе, инфаркте легкого.
Лейкоциты в небольшом количестве встречаются в любой мокроте. Большое количество нейтрофилов отмечается в слизисто-гнойной и особенно в гнойной мокроте. Эозинофилами богата мокрота при бронхиальной астме, эозинофильной пневмонии, гельминтозах легких, инфаркте легкого, туберкулезе и раке легкого. Лимфоциты встречаются в большом количестве при коклюше. Увеличение содержания лимфоцитов в мокроте возможно при туберкулезе легких.
Обнаружение единичных эритроцитов в мокроте диагностического значения не имеет. Появление большого количества эритроцитов в мокроте отмечается при состояниях, сопровождающихся кровохарканьем и легочным кровотечением. При наличии свежей крови в мокроте определяются неизмененные эритроциты, если же с мокротой отходит кровь, задержавшаяся в дыхательных путях в течение длительного времени, то обнаруживают выщелоченные эритроциты.
Эластические волокна появляются в результате распада легочной ткани при туберкулезе, абсцессе, гангрене легкого, раке легкого. При гангрене легкого эластические волокна обнаруживают не всегда, так как под действием ферментов, находящихся в мокроте, они могут растворяться. Спирали Куршмана — особые трубчатые тела, обнаруживаемые при микроскопическом исследовании, а иногда видимые невооруженным глазом. Обычно спирали Куршманна определяются при бронхиальной астме, туберкулезе легких и пневмонии. Кристаллы Шарко—Лейдена обнаруживаются в мокроте, богатой эозинофилами при бронхиальной астме, эозинофильной пневмонии.
Вскрытие петрифицированного туберкулезного очага в просвет бронха может сопровождаться одновременным обнаружением в мокроте обызвествленных эластических волокон, кристаллов ХС, МБТ и аморфной извести (так называемая тетрада Эрлиха) — 100%.
Исследование мокроты на микобактерии туберкулеза (МБТ) производится в специально окрашенном мазке. Установлено, что обычное исследование окрашенного мазка на МБТ дает положительный результат только при содержании МБТ не менее 50 000 в 1 мл мокроты. По количеству обнаруженных МБТ судить о тяжести процесса нельзя.
При бактериоскопии мокроты больных с неспецифическими заболеваниями легких могут быть обнаружены:
- при пневмониях — пневмококки, диплококки Френкеля, бактерии Фридлендера, стрептококки, стафилококки — 100%;
- при гангрене легкого — веретенообразная палочка в сочетании со спирохетой Венсана — 80%;
- дрожжеподобные грибы, для выяснения вида которых необходим посев мокроты — 70%;
- при актиномикозе — друзы актиномицета — 100%.
Объем трахеобронхиального секрета в норме колеблется от 10 до 100 мл/сут. Все это количество здоровый человек обычно проглатывает, того не замечая. В норме количество лейкоцитов в мокроте небольшое. В норме исследование окрашенного мазка на МБТ дает отрицательный результат.
При абсцессе легкого выделяется большое количество мокроты. Увеличение количества мокроты расценивается как признак ухудшения состояния больного. Мокрота может быть слизисто-гнойной, чисто гнойной, кровавой. Запах мокроты — гнилостный (трупный). Наличие гноя придает мокроте зеленоватый оттенок. При стоянии гнойная мокрота обычно разделяется на 2 слоя. При прорыве абсцесса печени в легкое из-за сообщения между печенью и легким в мокроте могут обнаруживаться желчные пигменты. В результате распада легочной ткани при абсцессе в мокроте появляются эластические волокна.
При бронхоэктатической болезни выделяется большое количество мокроты. Увеличение количества мокроты расценивается как признак ухудшения состояния больного. Мокрота может быть слизистой, слизисто-гнойной, чисто гнойной, кровавой. Наличие гноя придает мокроте зеленоватый оттенок. Запах мокроты — гнилостный (трупный). При стоянии гнойная мокрота обычно разделяется на 2 слоя.
При гангрене легкого выделяется большое количество мокроты. Увеличение количества мокроты расценивается как признак ухудшения состояния больного. Наличие гноя придает мокроте зеленоватый оттенок. Запах мокроты — гнилостный (трупный). Гнилостная мокрота часто разделяется на 3 слоя (верхний — пенистый, средний — серозный, нижний — гнойный). В мокроте могут встречаться пробки Дитриха, состоящие из продуктов распада бактерий и легочной ткани, кристаллов жирных кислот; эластические волокна, появляющиеся в результате распада легочной ткани. При гангрене легкого эластические волокна обнаруживают не всегда, так как под действием ферментов, находящихся в мокроте, они могут растворяться. При бактериоскопии мокроты могут быть обнаружены веретенообразная палочка в сочетании со спирохетой Венсана (80%).
При прорыве эмпиемы плевры в бронх мокрота чисто гнойная.
При абсцессе легкого выделяется большое количество мокроты. Увеличение количества мокроты расценивается как признак ухудшения состояния больного. Мокрота может быть слизисто-гнойной, чисто гнойной, кровавой. Запах мокроты — гнилостный (трупный). Наличие гноя придает мокроте зеленоватый оттенок. При стоянии гнойная мокрота обычно разделяется на 2 слоя. При прорыве абсцесса печени в легкое из-за сообщения между печенью и легким в мокроте могут обнаруживаться желчные пигменты. В результате распада легочной ткани при абсцессе в мокроте появляются эластические волокна.
При раке легкого выделяющаяся мокрота слизистая, кровавая. Слизисто-гнойная мокрота выделяется при раке легкого, сопровождающимся нагноением. При раке легкого, осложнившимся некрозом, мокрота приобретает гнилостный (трупный) запах. При бронхогенном раке легкого могут быть обнаружены клетки цилиндрического эпителия (как единичные, так и в виде скоплений). При раке легкого в мовроте могут быть обнаружены эозинофилы, опухолевые клетки, эластические волокна.
При сообщении пищевода с трахеей или бронхом, что может возникать при раке пищевода, в мокроте отмечается примесь только что принятой пищи.
В начале приступа бронхиальной астмы отделяется небольшое количество мокроты, в конце приступа ее количество увеличивается. Мокрота при бронхиальной астме слизистая. В ней могут быть обнаружены клетки цилиндрического эпителия (как единичные, так и в виде скоплений), эозинофилы, спирали Куршманна, кристаллы Шарко—Лейдена.
При острых бронхитах отделяется небольшое количество мокроты. Мокрота — слизистая. В ней могут быть обнаружены клетки цилиндрического эпителия (как единичные, так и в виде скоплений).
При хронических тонзиллитах из миндалин могут выделяться пробки, напоминающие по внешнему виду пробки Дитриха. Пробки из миндалин могут выделяться и при отсутствии мокроты.
При туберкулезном процессе в легком, сопровождающемся распадом ткани, особенно при наличии каверны, сообщающейся с бронхом, может выделяться много мокроты. Кровянистая мокрота, состоящая почти из чистой крови, наиболее часто отмечается при туберкулезе легких. При туберкулезе легких с творожистым распадом мокрота ржавого или коричневого цвета. В мокроте могут обнаруживаться фибринозные свертки, состоящие из слизи и фибрина; рисовидные тельца (чечевицы, линзы Коха); эозинофилы; эластические волокна; спирали Куршманна. Увеличение содержания лимфоцитов в мокроте возможно при туберкулезе легких. Определение белка в мокроте может явиться подспорьем при дифференциальной диагностике между хроническим бронхитом и туберкулезом: при хроническом бронхите в мокроте определяются следы белка, в то время как при туберкулезе легких в мокроте содержание белка больше, и он может быть определен количественно (до 100—120 г/л).
При силикозе легких в мокроте определяется примесь крови.
При коклюше в мокроте в большом количестве встречаются лимфоциты.
При туберкулезном процессе в легком, сопровождающемся распадом ткани, особенно при наличии каверны, сообщающейся с бронхом, может выделяться много мокроты. Кровянистая мокрота, состоящая почти из чистой крови, наиболее часто отмечается при туберкулезе легких. При туберкулезе легких с творожистым распадом мокрота ржавого или коричневого цвета. В мокроте могут обнаруживаться фибринозные свертки, состоящие из слизи и фибрина; рисовидные тельца (чечевицы, линзы Коха); эозинофилы; эластические волокна; спирали Куршманна. Увеличение содержания лимфоцитов в мокроте возможно при туберкулезе легких. Определение белка в мокроте может явиться подспорьем при дифференциальной диагностике между хроническим бронхитом и туберкулезом: при хроническом бронхите в мокроте определяются следы белка, в то время как при туберкулезе легких в мокроте содержание белка больше, и он может быть определен количественно (до 100—120 г/л).
При острых бронхитах мокрота слизистая. В ней могут быть обнаружены клетки цилиндрического эпителия (как единичные, так и в виде скоплений).
При легочной форме сибирской язвы мокрота может быть ржавой или коричневого цвета, что указывает на содержание в ней не свежей крови, а продуктов ее распада (гематин).
При пневмониях отделяется небольшое количество мокроты. По характеру она может быть слизистой, слизисто-гнойной. Примесь крови в мокроте определяется при крупозной и очаговой пневмониях. Мокрота ржавого или коричневого цвета, указывает на содержание в ней не свежей крови, а продуктов ее распада (гематин) и встречается при крупозной пневмонии. Желто-канареечный цвет имеет иногда мокрота при эозинофильных пневмониях. В мокроте могут быть обнаружены фибринозные свертки, состоящие из слизи и фибрина; желчные пигменты, что связано с внутрилегочным распадом эритроцитов и последующими превращениями гемоглобина; эозинофилы (при эозинофильной пневмонии); спирали Куршманна; кристаллы Шарко—Лейдена (при эозинофильной пневмонии); пневмококки, диплококки Френкеля, бактерии Фридлендера, стрептококки, стафилококки (100%).
Отмечается много свежих эритроцитов, сидерофагов, гемосидерина.
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
НИИ пульмонологии МЗ РФ, Москва
НИИ пульмонологии МЗ РФ, Москва
Г иперэозинофилия встречается при большой группе заболеваний, которые имеют разные механизмы возникновения, самые разнообразные клинические проявления и отличия в прогнозе и исходе. В клинической практике врачи многих специальностей имеют дело с больными, у которых повышено содержание эозинофилов в крови. Наиболее часто больные с гиперэозинофилией выявляются в практике пульмонологов и аллергологов. Однако данная диагностическая проблема не является редкостью при заболеваниях сердца и сосудов (системные васкулиты), у больных с неопластическими процессами. Особое место данный синдром занимает у больных с паразитарными, грибковыми, вирусными и другими заболеваниями (табл. 1). Описаны генетические врожденные формы гиперэозинофилии и идиопатический вариант ее возникновения. Ниже приводится рубрификация заболеваний, при которых может наблюдаться синдром гиперэозинофилии (P.Weller, 2002, Up–To–Date, Vol.10, №1). Каждый из разделов, приведенных в табл. 1, нуждается в самостоятельном анализе. Цель настоящего обзора – привлечь внимание врачей к проблеме гиперэозинофилии у больных с патологией дыхательной системы и рассмотреть дифференциально–диагностические алгоритмы при этой гетерогенной группе заболеваний. Общепринятой классификации заболеваний дыхательных путей при синдроме гиперэозинофилии не существует. Ниже приведены заболевания органов дыхания аллергической природы, сопровождающиеся гиперэозинофилией:
- Простая эозинофильная пневмония
Другую группу, при которых аллергические реакции не играют патогенетической роли, составляют разнообразные по клиническим проявлениям заболевания с поражением органов дыхания. Так, к этой группе может быть отнесен гистиоцитоз Х, лимфомы и лимфогранулематоз, инфекционные заболевания негельминтной природы (СПИД, цитомегаловирусная инфекция) и др.
Под гиперэозинофильным синдромом понимают повышение числа эозинофилов в периферической крови свыше 250 клеток в 1 мкл. Физиологическая норма колеблется от 50 до 250 эозинофилов в 1 мкл. Критическим уровнем, который указывает на патологический процесс, связанный с увеличением числа эозинофилов, является уровень клеток, превышающий 450 в 1 мкл. При этом необходимо подчеркнуть, что уровень эозинофилов крови может не коррелировать с тканевой эозинофилией и их содержанием в бронхоальвеолярном лаваже. Классическим примером может служить гистиоцитоз Х (его другое название – эозинофильная гранулема): эозинофильная инфильтрация обнаруживается только при гистологическом исследовании биоптатов легочной ткани, полученной при открытой биопсии, в то время как в крови эозинофилии не отмечается. При идиопатическом легочном фиброзе также повышенное содержание эозинофилов выявляется только при исследовании жидкости бронхоальвеолярного лаважа.
При диагностике причины гиперэозинофилии должны быть учтены все детали истории жизни и болезни пациента. Важна информация о его увлечениях (например, любитель птиц) и путешествиях (Африка, Латинская Америка и другие регионы, в которых распространены грибковые и паразитарные заболевания).
Предмет особого внимания – назначение лекарственных средств, при приеме которых наиболее часто встречаются гиперэозинофильные реакции. К ним относят: нитрофураны, фенитоин, альфа–триптофан, ампициллин, ацетаминофен, пентамидин (при ингаляционном способе введения), ранитидин, колониестимулирующий фактор гранулоцитов–моноцитов, силикат алюминия и другие соли металлов. Следут выделить серосодержащие соли, которые используют при возделывании виноградников, наркотики (героин, кокаин), аллергию на латекс у рабочих резиновой промышленности и другие.
Реакция легочной ткани на прием лекарственных средств в настоящее время вызывает все большую озабоченность медиков. В последние годы были описаны гиперэозинофильные реакции и легочные инфильтраты при назначении кортикостероидных гормональных препаратов, кромогликата натрия и некоторых других перапаратов. Иммунологические механизмы аллергических реакций, возникающих на прием лекарственных средств, охарактеризованы недостаточно. Они чаще всего не зависят от иммуноглобулина класса Е.
Клинически патологическая реакция органов дыхания может протекать, как остро возникшее заболевание, или развиваться медленно, приобретая черты хронического процесса. В последнем случае всегда возникают диагностические сложности, так как порой бывает трудно установить причинную связь между симптомами болезни и длительным приемом лекарственного средства. В этом плане лучше известны побочные эффекты нитрофуранов. Так, описаны гиперэозинофильные легочные инфильтраты, возникшие после их приема; при длительном назначении возможно развитие волчаночно–подобного синдрома (J. Murray, J. Nadel, 1988).
Наиболее частыми реакциями со стороны органов дыхания могут быть эозинофильные пневмонии, альвеолит, интерстициальная пневмония, бронхиальная астма. Таким образом, врачу, который лечит больного с гиперэозинофилией, необходимо самым тщательным образом собрать лекарственный анамнез. Он должен провести своеобразную ревизию всех лекарственных средств, назначенных врачами самых разнообразных специальностей, а также точно знать, какие препараты больной принимал сам, без ведома врачей. Данное правило является одним из необходимых условий успешной диагностики и эффективного лечения.
Физикальное обследование несет очень важную диагностическую информацию о поражении нижнего или верхнего отделов дыхательных путей. Принципиальное значение в постановке диагноза имеет обнаружение симптомов, свидетельствующих о поражении не только легких, но и других органов и систем (сердце, центральная нервная система, почки, опорно–мышечный аппарат и другие). Клиническое обследование должно ориентировать врача на проведение рациональной диагностической программы, включая современные методы лабораторной и имидж–диагностики, иммуногистохимические и гистологические исследования.
Диагностический поиск при гиперэозинофилии должен быть направлен на обнаружение симптомов, свидетельствующих о мультиорганном патологическом процессе. Если клинический осмотр выявляет поражение не только легких, но и сердца, печени, селезенки, мышц, фасций, и других органов и систем, то речь, как правило, может идти о неаллергических системных заболеваниях или же идиопатическом гиперэозинофильном синдроме. В этом плане важным диагностическим признаком является высокая СОЭ, не характерная для аллергических заболеваний. При обследовании больных с гиперэозинофилией всегда обращают внимание на ее сочетание с повышением концентрации IgE, что в большей степени характерно для аллергических заболеваний, некоторых форм первичного системного васкулита (синдром Чардж – Стросса), а также грибковых заболеваний.
Простая эозинофильная пневмония
Простую эозинофильную пневмонию отождествляют с синдромом Леффлера. В 1932 году Леффлер опубликовал работу, посвященную дифференциальной диагностике легочных инфильтратов. Он описал четырех пациентов, у которых клиническая картина характеризовалась минимальными проявлениями со стороны дыхательных путей, гиперэозинофилией и самостоятельно разрешающимися инфильтратами, которые диагностировались только при рентгенографии органов грудной клетки. Ретроспективный анализ больных с простой эозинофильной пневмонией позволяет рассматривать клиническую картину более глубоко. Так, у больных часто появляются сухой непродуктивный кашель, хрипы в грудной клетке, по большей части в ее верхних отделах, ощущение легкой боли в области трахеи, что связывают с раздражением ее слизистой при прохождении личинок аскарид или других паразитов. Мокрота носит вязкий характер и может иметь легкий кровянистый оттенок. При рентгенографии легких выявляются инфильтраты округлой или овальной формы от нескольких миллиметров до нескольких сантиметров в обоих легочных полях. Эти инфильтраты сопровождаются увеличением числа эозинофилов в периферической крови до 10%. Инфильтраты держатся несколько недель, могут мигрировать по легочным полям и самостоятельно разрешиться, не оставив рубцовых изменений в легочной ткани.
Наиболее часто простая эозинофильная пневмония вызывается такими паразитами, как Ascaris lumbricoides, Strongyloides stercoralis, Ancylоstoma, Necator, Uncinaria. Личинки этих паразитов током крови могут доставляться в дыхательные пути, а затем, в конечном счете, – в желудочно–кишечный тракт. Рекомендуется проводить исследование мокроты и кала на предмет обнаружения личинок паразитов.
В мокроте обнаруживается повышенное содержание эозинофилов и продуктов их деградации – кристаллов Шарко–Лейдена. Диагностическое значение приобретает также повышение уровня IgE, как правило, выше 1000 единиц. Обнаружение такого высокого уровня IgE всегда побуждает исключать паразитарное или же грибковое заболевание. Гиперэозинофилия и гипериммуноглобулинемия (IgE) являются реакциями, направленными на элиминацию паразитов из организма. Эозинофилы секретируют такие пептиды, как эозинофильная пероксидаза, катионный протеин, большой основной белок, а также перекись водорода и другие биологически активные субстанции. Возрастает поляризация Th2 клеток, что приводит к повышенной секреции интерлейкина 5 и продукции IgE.
Патогенетические механизмы объясняют основные клинические проявления простой эозинофильной пневмонии. Так, становится понятным, почему появляется кашель, характер мокроты, хрипы в грудной клетке, гиперэозинофилия крови и мокроты, гипериммуноглобулинемия IgE, летучий характер эозинофильных инфильтратов.
W. Thurlbleck, A. Churg (1995) приводят случаи эозинофильной пневмонии, протекавшей по типу синдрома Леффлера и инициированные приемом сульфонамидов; в других сериях причиной пневмонии явились соли никеля, которые используются при чеканке монет.
Другие формы легочной патологии обусловлены инвазией паразитов непосредственно в легочную ткань, чем объясняют продолжительные клинические проявления эозинофильных инфильтратов. К такой форме паразитарной патологии относится парагонимоз (Paragonimus westermani, род нематод). Взрослые особи мигрируют через стенку кишки и диафрагмы в легочную ткань, индуцируя воспалительную реакцию. Исходом воспалительного процесса в легких является образование фиброзных участков, содержащих один–два гельминта. Фиброзные узлы могут сливаться, образуя участки кистозного перерождения легочной ткани. Особенностью клинической картины при парагонимозе является вовлечение в патологический процесс плевральной полости. Экссудат плевральной полости и инфильтрированная легочная ткань содержат преимущественно эозинофилы. Мокрота приобретает шоколадный оттенок, в ней часто присутствуют прожилки крови. Высокое содержание эозинофилов в крови наблюдается в начале заболевания, однако при хронических формах оно может быть в пределах нормальных величин.
Наконец, третьей формой паразитарного поражения легких и других органов человеческого организма является массивное проникновение личинок и яиц паразитов в ткани. В результате гематогенной диссеминации в легкие личинок и яиц развиваются кашель, хрипы, одышка. Для острых воспалительных реакций характерно увеличение числа эозинофилов в крови. Подобного типа воспалительные реакции наблюдаются при массивном проникновении личинок аскарид, трихин, шистосом, а также при стронгилоидозе. Среди паразитарных эозинофильных форм легочной патологии особое место занимают тропические формы, которые вызываются такими филяриями, как Wuchereria bancrofti, Brugia malayi.
Таким образом, простая эозинофильная пневмония чаще всего развивается при паразитарных заболеваниях и приеме некоторых лекарственных средств. Она характеризуется минимальными проявлениями бронхолегочного синдрома, гиперэозинофилией, гипергаммаглобулинемией IgE и «летучими» легочными инфильтратами. Прогноз благоприятен; как правило, не требуется назначения глюкокортикостероидов, поскольку происходит спонтанное разрешение инфильтратов. Бесспорно, у данной категории больных необходимо проводить дегельминтизацию. Другие формы паразитарного поражения легких отличаются клиническими проявлениями и механизмами патологических процессов. Эта группа легочной патологии также протекает с эозинофилией, что необходимо учитывать при проведении дифференциальной диагностики.
Острая эозинофильная пневмония
Острая эозинофильная пневмония (ОЭП) является своеобразным антиподом простой эозинофильной пневмонии. Она протекает с симптомами острой дыхательной недостаточности, угрожающей жизни больного человека. В клинической картине имеется много общего с десквамативной пневмонией и с респираторным дистресс–синдромом взрослых. Отличительной особенностью ОЭП является обнаружение более 40% эозинофилов в бронхоальвеолярной жидкости и хороший прогноз при назначении глюкокортикостероидов. Болезнь начинается остро, в течение 1-5 дней, драматически нарастают симптомы острой дыхательной недостаточности. По жизненным показаниям начинается искусственная вентиляция легких. Реанимационным мероприятиям предшествует короткий период, когда больные жалуются на боль в грудной клетке без определенной локализации, мышечную боль, повышенную температуру тела.
При обследовании могут выслушиваться крепитирующие «целлофановые» хрипы. При рентгенологическом обследовании органов грудной клетки выявляются интенсивные смешанной природы инфильтраты, которые распространяются как на альвеолярное, так и интерстициальное пространство. Локализация инфильтратов самая разнообразная, но преимущественно – в верхних отделах легких (при хронической эозинофильной пневмонии инфильтраты локализуются в основном на периферии легких). Количество эозинофилов в периферической крови, как правило, нормальное, что особенно контрастирует с высоким их содержанием в бронхоальвеолярной жидкости – от 12 до 44%, тогда как в норме определяют единичные клетки. Попытки установить инфекционную природу безуспешны, даже если проведена биопсия легочной ткани, так же как не удается увязать происшедшие изменения с приемом лекарственных средств. Компьютерная томография высоких разрешений выявляет диффузные консолидирующиеся инфильтраты, которые распространяются на альвеолярное пространство и захватывают интерлобарные перегородки. Инфильтративный процесс часто распространяется на плевру. Данный признак может быть использован в дифференциальном диагнозе ОЭП с идиопатическим интерстициальным фиброзом легких. Плевральное повреждение более чем в 50% случаев сопровождается образованием экссудата в плевральной полости, чаще всего бывает двухстороннего. Важным подспорьем в постановке окончательного диагноза является быстрое исчезновение инфильтратов: в течение нескольких дней после назначения глюкокортикостероидов.
Патологические особенности ОЭП были изучены Davis et al. (1986), описавшими идиопатическую форму острой дыхательной недостаточности, для которой характерным оказалось высокое содержание эозинофилов в бронхоальвеолярном лаваже. Другая особенность состояла в том, что был хороший ответ на терапию глюкокортикостероидами без последующего обострения заболевания. Болезнь протекала остро, в дальнейшем рецидива не наблюдалось. В анамнезе не было никаких сведений о наличии бронхиальной астмы. Таким образом, при развитии ОЭП были исключены инфекционные заболевания дыхательных путей, бронхиальная астма и не было установлено связи с приемом известного лекарственного средства, что давало основание рассматривать эту форму патологии, как идиопатическую.
Tazelaar et al. описали морфологические особенности ОЭП (рис. 1). Они указали на острое и диффузное геморрагическое поражение альвеол с выраженной инфильтрацией эозинофилами, которые депонировались в альвеолах и интерстиции. Отмечались гиалиновые мембраны и гиперплазия пневмоцитов второго типа.
Рис. 1. Острая эозинофильная пневмония
Дифференциальный диагноз проводится с диффузным альвеолярным повреждением, острой интерстициальной пневмонией и хронической эозинофильной пневмонией. Отличительной чертой является обнаружение при ОЭП кластеров эозинофилов (5–10 клеток в поле зрения). От хронической эозинофильной пневмонии она отличается продолжительностью клинических проявлений болезни, т.е. в основе дифференциального диагноза лежат особенности клинической картины этих форм пневмонии.
Хроническая эозинофильная пневмония
Термин хроническая эозинофильная пневмония (ХЭП) был введен в клиническую практику Carrington et al. в 1969 г. Авторы наблюдали группу больных из девяти человек, все они были женщины в возрасте около пятидесяти лет. Основные клинические проявления – снижение веса, ночные поты, нарастающая в своей интенсивности одышка. Шесть женщин из девяти страдали бронхиальной астмой, но характер одышки у них существенно изменился и присоединились симптомы общей интоксикации. Особое внимание привлекли изменения, выявленные при проведении рентгенографии органов грудной клетки. У всех больных были выявлены легочные инфильтраты, расположенные по периферии, так что создавалось впечатление о наличии жидкости в плевральной полости. В последующие годы к этой клинической проблеме возвращались многие авторы (J. Murray, J. Nadel, 1988; M. Thurlbeck, A. Churg, 1995 и другие). К тому времени сформировалась клиническая концепция хронической эозинофильной пневмонии. Болезнь не протекает так остро и с признаками острой дыхательной недостаточности, как это наблюдается при ОЭП. Другая отличительная особенность, что важно учитывать при дифференциальной диагностике с простой эозинофильной пневмонией – легочные инфильтраты спонтанно не разрешаются, и больные с ХЭП нуждаются в лечении. Наконец, при этой форме пневмонии установлены характерные рентгенологические и морфологические изменения, что и предопределило правомерность выделения этой категории больных.
Итак, основные клинические проявления ХЭП – кашель, одышка, повышение температуры тела, потливость, снижение массы тела, реже – продукция мокроты, кровохарканье. Около 50% больных в анамнезе имеют указание на бронхиальную астму, у большинства из них выявляется эозинофилия периферической крови. Высокое содержание эозинофилов отмечается при исследовании мокроты. Важное диагностическое значение имеет обнаружение эозинофилов в бронхоальвеолярном лаваже, которые могут доминировать над другими клетками. Проведение бронхоальвеолярного лаважа является необходимой диагностической процедурой у больных с ХЭП.
Причина возникновения ХЭП остается мало изученной, поэтому ее рассматривают, как идиопатическое заболевание. В последние годы появились сообщения о роли лекарственных средств, индуцирующих ее возникновение. В эту группу лекарственных препаратов внесены блеомицин, нитрофураны, парааминосалициловая кислота, пенициллин, сульфаниламиды, L–триптофан, а также кокаин, соли никеля. Выше уже обсуждалась необходимость самой тщательной ревизии лекарственных препаратов, которые были назначены больному с гиперэозинофилией.
Большим подспорьем в постановке диагноза служат рентгенологические методы (рис. 2). При рентгенографии органов грудной клетки у большинства больных выявляются периферические, не сегментарные, облаковидные инфильтраты, иногда – феномен «матового стекла». Они преимущественно локализуются в области верхушек легких и чаще аксиллярно. Компьютерная томография легких позволяет получить более точную диагностическую информацию о локализации инфильтратов, их распространенности и связи с плеврой.
Рис. 2. Хроническая эозинофильная пневмония
Патоморфологические изменения при ХЭП (рис. 3) характеризуются скоплением в альвеолярном пространстве альвеолярных макрофагов с заметным увеличением числа эозинофилов. Макрофаги содержат фагоцитируемые ими гранулы эозинофилов. На ранних стадиях заболевания наблюдается белковый экссудат в межальвеолярных перегородках, с формированием эозинофильных абсцессов и появлением гистиоцитов. Отмечается гиперплазия пневмоцитов второго типа, которая сопровождается воспалительными реакциями интерстициальной ткани.
Рис. 3. Хроническая эозинофильная пневмония
Достаточно сложной областью является дифференциальная морфологическая диагностика ХЭП с синдромом Чардж–Стросса, эозинофильной гранулемой, десквамативной интерстициальной пневмонией и гранулематозом Вегенера. Отличительной морфологической чертой синдрома Чардж–Стросса являются признаки гранулематозного васкулита и развитие некротической гранулемы, что не характерно для больных с хронической эозинофильной пневмонией. При эозинофильной гранулеме преобладают изменения в интерстициальной легочной ткани, в которой заметно возрастает число гистиоцитов, появляются клетки Langerhans, а также эозинофилы. Десквамативная интерстициальная пневмония, описанная А.А. Liebow, характеризуется аккумуляцией альвеолярных макрофагов в альвеолярном пространстве. Эозинофилы при этой форме воспалительной реакции не определяются. Гранулематоз Вегенера характеризуется развитием ангиоцентрической гранулемы, которая осложняется асептическим некрозом. Наконец, следует указать на морфологические отличия при инфекционных легочных процессах, при которых удается идентифицировать патоген, что исключает идиопатическую природу ХЭП.
Лечебная программа при ХЭП основана на применении глюкокортикостероидов. Однако следует подчеркнуть, что приблизительно у 10% больных выздоровление наступает без применения каких-либо лекарственных средств. Учитывая подострое течение болезни и возможность спонтанного разрешения воспалительного процесса, необходимо проявлять сдержанность при назначении медикаментозной терапии. В практическом смысле это означает, что больные нуждаются в проведении доказательной диагностики, динамического наблюдения за течением болезни, и только после этого решается вопрос о назначении глюкокортикостероидов.
Адекватная инициальная терапия у больных с хронической эозинофильной пневмонией основана на применении преднизолона в дозе от 40 до 60 мг в сутки. Данная доза сохраняется в течение 2-6 недель до полного разрешения инфильтратов в легочной ткани, после чего суточная доза преднизолона снижается до 20–30 мг в сутки и продолжается еще восемь недель. Подобная жесткая схема назначения системных глюкокортикостероидов продиктована тем, что у этой категории больных достаточно часто происходит обострение болезни (по типу синдрома отмены). Рекомендуется прибегать к альтернирующей схеме назначения глюкокортикостероидов. Если болезнь осложняется развитием симптомов острой дыхательной недостаточности, то рекомендуется прибегать к пульс–терапии. С этой целью используется метилпреднизолон, который назначают в дозе 250 мг в/в каждые 6 часов, сочетая с приемом препаратов per os.
Обострение заболевания происходит более чем у 80% больных ХЭП и наблюдается в сроки от нескольких месяцев до года. При обострении заболевания необходимо вернуться к исходным дозам глюкокортикостероидов, чтобы добиться хорошего контроля над течением заболевания. Ингаляционные глюкокортикостероиды во время «пика» заболевания не рекомендуется назначать; их применяют в период снижения дозы преднизолона, с тем чтобы предотвратить развитие синдрома отмены.
Критериями эффективности проводимой терапии являются исчезновение одышки, нормализация температуры, снижение числа эозинофилов в периферической крови. При контрольном рентгенологическом исследовании органов грудной клетки большинство инфильтратов в течение короткого времени подвергаются обратному развитию. Обычно при правильно подобранной дозе преднизолона и чувствительности к нему процесс разрешается в течение двух недель. Более чувствительным методом в оценке эффективности терапии преднизолоном является компьютерная томография, которая позволяет проследить этапы разрешения пневмонии. В оценке эффективности терапии большое значение имеет нормализация числа эозинофилов в периферической крови и их исчезновение в бронхиальном секрете, снижение уровня IgЕ и нормализация СОЭ.
Клиническая проблема состоит в предупреждении нежелательных побочных эффектов при проведении терапии преднизолоном. Обычно лечение рекомендуется проводить в течение 6-9 месяцев. Прогноз считается неблагоприятным, если при указанной тактике ведения больного с ХЭП наступает обострение заболевания.
Идиопатический гиперэозинофильный синдром
Идиопатический гиперэозинофильный синдром (ИГЭС) характеризуется длительным повышением числа эозинофилов в периферической крови и инфильтрацией этими клетками многих органов и тканей, что и обусловливает клиническую картину мультиорганного повреждения. Данный синдром относится к числу гетерогенных по своим клиническим проявлениям и исходам, что, видимо, связано с различными причинами его возникновения и патогенетическими механизмами. Однако современное знание этой проблемы не позволяет разграничить возможно разные болезни, которые сегодня объединены в одну рубрику ИГЭС.
В постановке диагноза клиницисты ориентируются на следующие признаки: эозинофилия периферической крови более 1500/мкл, сохраняющаяся в течение более чем шести месяцев; исключены такие причины, как паразитарная инфекция и аллергические заболевания; симптомы мультиорганного патологического процесса. Указанные критерии свидетельствуют о том, что клиницисту при постановке диагноза ИГЭС необходимо исключить большую группу заболеваний, при которых происходит повышение числа эозинофилов. Иначе говоря, диагностический процесс построен по принципу исключения как известных, так и идиопатических заболеваний с гиперэозинофилией.
Клиническая картина синдрома проявляется такими неспецифическими симптомами, как общее недомогание, кашель (как правило, непродуктивный), мышечные боли, ангионевротический отек, крапивница, повышение температуры тела, нарушение зрения. Поражение сердечно–сосудистой системы, нервной системы и селезенки происходит более чем у 80% больных; реже можно наблюдать патологические изменения со стороны печени, желудочно–кишечного тракта, органа зрения.
Ключевую роль в постановке диагноза играет подсчет числа лейкоцитов и формулы крови. Так, число лейкоцитов у отдельных больных повышается до 90000 и более, что всегда побуждает исключать лейкоз. Высокое содержание среди прочих клеток белой крови приходится на зрелые формы эозинофилов, однако у части больных появляются и клетки–предшественники эозинофилов. Исследование костного мозга демонстрирует его обогащение как зрелыми формами эозинофилов, так и их предшественниками. Хромосомных и цитогенетических изменений при ИГЭС не описано.
Прогностически неблагоприятным признаком считается поражение сердца, так как это может стать причиной инвалидности, а при особенно тяжелых формах патологического процесса – и непосредственной причиной смерти. В клинической картине можно выделить три фазы поражения миокарда. Начальная стадия описывается, как стадия острого некроза; интермиттирующая стадия, следующая за некротической, характеризуется образованием внутрисердечных тромбов, которые формируются на месте развившегося ранее некроза; наконец, третья стадия – фибротическая. Острая стадия некроза миокарда развивается в первые полтора месяца от развития гиперэозинофильного синдрома. Повреждение эндомиокарда происходит вследствие его инфильтрации лимфоцитами и эозинофилами; из гранул последних выделяется значительное число веществ, приводящих к некрозу кардиомиоцитов и формированию асептических микроабсцессов миокарда. На этой стадии заболевания клинические проявления минимальны, и лишь только происшедшая тромбоэмболия и активный поиск ее источника могут выявить признаки повреждения миокарда, наступившего вследствие эозинофильной инфильтрации эндомиокарда и развившегося некротического процесса. Начальные проявления эозинофильной инфильтрации могут подтверждаться биопсией эндомиокарда, так как другие диагностические методы малоспецифичны и малочувствительны в диагностике поврежденного миокарда. Клиницистам данная категория больных больше известна по стадии массивной тромбоэмболии или же стадии фиброза миокарда, когда формируется рестриктивная кардиомиопатия и выраженная регургитация через митральный и трикуспидальный клапаны.
Неврологические симптомы у больных с ИГЭС могут возникнуть вследствие тромбоэмболии сосудов головного мозга, а также проявиться симптомами энцефалопатии или периферической нейропатии. Церебральная тромбоэмболия возникает вследствие заноса тромба из полости сердца и проявляется в виде инсульта или же преходящих ишемических эпизодов. Терапия антикоагулянтами, как правило, не приносит желаемого эффекта, так как эмболии могут рецидивировать несмотря на нее. Энцефалопатия проявляется изменениями в сфере сознания, снижением памяти, возможно развитие атаксии. У некоторой части больных появляются признаки поражения моторных нейронов, о чем свидетельствует возрастающий мышечный тонус, положительный рефлекс Бабинского. Периферическая нейропатия возникает приблизительно у каждого второго больного с ИГЭС в виде изменения чувствительности и атрофии мышц. О природе развивающейся нейропатии пока мало что известно.
Патологические изменения со стороны кожных покровов являются достаточно частой клинической проблемой у больных с ИГЭС. Больные часто обращаются по поводу ангионевротических отеков, уртикарных и эритематозных высыпаний, образования зудящих папул и узелков. В основе возникновения кожных симптомов лежит периваскулярная инфильтрация эозинофилами, в меньшей степени – нейтрофилами. Развитие кожных симптомов, таких как ангионевротический отек, уртикарные высыпания, относится к числу признаков, которые свидетельствуют о благоприятном течении болезни. Они достаточно быстро регрессируют при назначении терапии глюкокортикостероидами.
Разнообразны по своим клиническим проявлениям изменения, которые наблюдаются со стороны органов дыхания. Больные часто жалуются на появление непродуктивного кашля, одышку, но бронхиальная астма не является характерным признаком для больных с ИГЭС. При рентгенологическом исследовании часто выявляются инфильтраты, возникающие вследствие миграции эозинофилов в паренхиму легких. При далекозашедших стадиях возможно развитие фиброза легочной ткани или инфарктных пневмоний.
Другие органы и системы в патологический процесс при ИГЭС вовлекаются реже. Автор наблюдал больную, у которой была диагностирована эозинофильная инфильтрация слизистой желудка, кишечника; в клинику она обратилась по поводу обострения бронхиальной астмы и гиперэозинофильного синдрома. Отдаленное наблюдение за больной выявило поражение клапанного аппарата сердца и развитие признаков застойной сердечной недостаточности.
Дифференциальная диагностика при автора проводится с паразитарными и грибковыми заболеваниями, острой эозинофильной лейкемией, синдромом Чардж–Стросса.
Лечебная программа включает назначение глюкокортикостероидов только на этапе мультиорганного поражения. На начальных этапах заболевания, когда выявляется высокое содержание эозинофилов в крови и отсутствуют признаки поражения сердца, легких, нервной системы, кожных покровов, рекомендуется ограничиться только наблюдением за больными. Терапия глюкокортикостероидами дополняется назначением циклоспорина, интерферона- a в тех случаях, когда в клинической картине появляются признаки мультиорганной патологии и низкой эффективности преднизолона.
Бронхиальная астма (БА) относится к числу заболеваний, которые распространены в современном обществе и сохраняют тенденцию к дальнейшему росту. Болезнь определяется, как хроническое воспалительное заболевание дыхательных путей, которое протекает при участии большого количества клеток, но доминирующая роль принадлежит эозинофилам. Ведущие проявления – приступы одышки, кашель, повышенная продукция вязкого бронхиального секрета. Эти клинические признаки обусловлены преходящей обструкцией дыхательных путей, возникающей вследствие спазма гладких мышц бронхов, отека слизистой дыхательных путей и образования вязкого секрета, способного обтурировать их проходимость. У больных БА, умерших на высоте status asthmaticus, при проведении аутопсии обнаруживают выраженную гиперинфляцию, легочная ткань не коллабирует после вскрытия грудной клетки, так как просвет особенно мелких по диаметру бронхов обтурирован слизистыми пробками. Они в виде слепков часто воспроизводят анатомическую структуру бронхов. Эозинофилы – основные клетки, которые входят в состав детрита слизистой пробки. Другими элементами слизистой пробки являются спирали Куршмана, десквамированный эпителий с тельцами Креола.
При гистологическом исследовании обращает на себя внимание возросшее число бокаловидных клеток, которые находятся в состоянии гипертрофии. Морфологическим маркером БА является утолщение базальной мембраны, которая превышает 17 микрон (при норме не более 7 микрон). Эти изменения в базальной мембране обусловлены отложением коллагена IV типа, но не депозитами, состоящими из иммуноглобулинов. Особое внимание уделяется гипертрофии гладких мышц бронхов, степень которой коррелирует с тяжестью течения БА. Необходимо подчеркнуть, что аккумуляция эозинофилов в толще стенки бронхов при БА не сопровождается появлением легочных эозинофильных инфильтратов, развитием мультиорганной патологии.
Маркером БА является повышение концентрации оксида азота в выдыхаемом воздухе, которое наблюдается только лишь при этой патологии, может служить дифференциально-диагностическим тестом при гиперэозинофильном синдроме. Из большой группы легочных заболеваний повышение концентрации оксида азота происходит только у больных БА.
Ингаляционные глюкокортикостероиды рассматриваются, как базисная терапия при лечении больных, страдающих БА средней и тяжелой степени тяжести (в отличие от других форм легочной патологии, которые сопровождаются повышенным содержанием эозинофилов в мокроте и крови).
Аллергический ринит (АР) часто рассматривают, как состояние, которое предшествует развитию бронхиальной астмы. При АР сравнительно часто отмечается повышение числа эозинофилов как в периферической крови, так и в секрете, полученном из носа. Топическая эозинофилия носового секрета не коррелирует с уровнем эозинофилов в периферической крови. В плане дифференциальной диагностики необходимо учитывать, что бронхиальная астма может возникать без симптомов предшествующего аллергического ринита.
Полипы слизистой носа возникают как у больных с нарушенной толерантностью к аспирину и нестероидным противовоспалительным препаратам (аспириновая бронхиальная астма), так и у больных без признаков бронхиальной астмы.
Наконец, выделен неаллергический ринит, который протекает с повышенным содержанием эозинофил
источник