Все опухоли можно разделить на доброкачественные и злокачественные. Первые растут, «раздвигают» ткани, но не разрушают их, имеют капсулу, четкие границы, не метастазируют и не рецидивируют. Злокачественные в значительной степени определяются особенностями их клеток: автономностью и бесконтрольностью роста, анаплазией и атипизмом, способностью вторгаться в другие органы и прорастать в них, метастазированием.
По данным канцер-регистра, с 2008 г. в Беларуси ежегодно выявляется свыше 40 000 случаев злокачественных новообразований с впервые установленным диагнозом. Пациенты с опухолями злокачественной природы (за исключением базалиомы кожи) пожизненно состоят на диспансерном учете из-за риска рецидивирования и развития повторных (первично-множественных) новообразований. При такой болезни человек цепляется за любое лекарство или процедуру как за спасительную соломинку. Многие спрашивают: а можно ли при раке делать физиопроцедуры?
Российский ученый, доктор мед. наук Геннадий Пономаренко выделяет 4 основные группы онкобольных, в лечении которых используются лечебные физические факторы:
• когда физиопроцедуры непосредственно воздействуют на опухоль;
• после радикальных операций — удаления злокачественных и доброкачественных опухолей (применяются в программах комплексного послеоперационного и восстановительного лечения);
• пациенты, которым физические факторы назначаются по поводу сопутствующих заболеваний после удаления новообразований;
• при неудаленных доброкачественных опухолях, склонных к малигнизации (мастопатия, киста придатков матки, фибромиома, доброкачественная гиперплазия предстательной железы и др.), когда физические факторы помогают лечить сопутствующие заболевания.
Для пациентов 1-й группы, наряду с онкодеструктивными (фотодинамическая терапия, высокоинтенсивные лазеро- и дециметровая терапия, ультразвуковая) и цитолическими методами (внутриорганный электрофорез цитостатиков), в комплексной терапии применяют воздействие, усиливающее работу препаратов химиотерапии.
Больным 2-й группы для профилактики осложнений назначают иммуносупрессивные (лекарственный электрофорез иммуносупрессантов) и химиомодифицирующие методы (низкочастотная магнитотерапия). После операции для профилактики лимфостаза применяют лимфодренирующие методы — пневматическую компрессию тканей конечностей, ЛФК, массаж. Далее для коррекции вегетативных расстройств используют вегетокорригирующие методы (электросонтерапия, транскраниальная электроанальгезия, гальванизация головного мозга, низкочастотная магнитотерапия). Пациентам с опухолями высокой степени малигнизации физиолечение назначают не после радикальной операции, а через более продолжительный интервал времени. У них удлиняют паузы между процедурами и курсами и снижают интенсивность действующих факторов. После тотального удаления доброкачественных опухолей противопоказания к физиопроцедурам только общие.
Сложнее с пациентами 3-й и 4-й групп. Они не всегда сообщают о наличии у них онкозаболевания, когда обращаются в различные медучреждения со своими сопутствующими хворями. Одни считают себя полностью выздоровевшими; другие не относят доброкачественные опухоли (мастопатия, киста придатков матки, фибромиома, доброкачественная гиперплазия предстательной железы и др.) к серьезным заболеваниям, третьи вообще скрывают свое онкологическое прошлое и просят дать им побольше всяких физиопроцедур.
Услышав о перенесенном ранее пациентом онкозаболевании, врачи нередко испытывают трудности. Как быть? Физиолечение в первую очередь не должно навредить.
После консультации онколога пациентам 3-й группы (при отсутствии роста тканей и метастазирования вне зоны удаленной опухоли) можно применять: УФО в определенных дозировках; ДДТ, СМТ по методикам обезболивания; электросон; электростимуляцию мышц; ультразвук; электрофорез лекарственных средств; ингаляции; ванны, души, гидрокинезотерапию (бассейн) индифферентной температуры; минеральные воды внутрь, в виде ингаляций, орошений, промываний; магнито-
терапию.
Больным 4-й группы противопоказаны воздействия в области локализации опухоли: тепловые процедуры, УФО, УЗ, высокочастотные факторы, массаж. Для других зон тела используют преимущественно низкоинтенсивные факторы или климатотерапию по щадящим режимам.
Светлана Трофимова, врач-реабилитолог РНПЦ онкологии и медрадиологии им. Н. Н. Александрова; Георгий Марушко, врач-реабилитолог 10-й ГКБ Минска.
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Рак гортани или подозрение на него являются показаниями к госпитализации.
Особенность планирования лечения рака гортани состоит в том, что необходимо не только излечить больного, но и восстановить голосовую, дыхательную и защитную функции гортани. На ранних стадиях заболевания полного выздоровления можно добиться с помощью лучевой терапии, органосохраняющих операций или сочетания этих методов.
Не следует догматически подходить к выполнению первоначального плана лечения. В процессе лучевой терапии выявляют одну из наиболее существенных характеристик опухоли — радиочувствительность. В зависимости от её выраженности производят коррекцию первоначального плана лечения.
Планирование лечения необходимо проводить на консилиумах хирургов, лучевых терапевтов, химиотерапевтов. При необходимости для участия в консилиуме приглашают эндоскопистов, рентгенологов и патоморфологов. Для обсуждения плана лечения необходимо располагать информацией о локализации опухоли в гортани, её границах, распространении на соседние отделы, преднадгортанниковое и околоскладочное пространство, форме роста, особенностях гистологического строения и морфологической дифференцировке. В процессе лечения к этим критериям добавляют информацию о радиочувствительности опухоли, оценивая степень уменьшения новообразования в процессе лучевой терапии. При биопсии после предоперационной лучевой терапии или микроскопического исследования после хирургического вмешательства правильность оценки этого критерия может быть проконтролирована при определении степени лучевого патоморфоза опухоли.
Рак среднего отдела гортани Т1-Т2 обладает высокой радиочувствительностью, поэтому лечение начинают с лучевой терапии. Лучевое лечение в предоперационном периоде (доза облучения 35-40 Гр) не ухудшает заживление тканей, если после него выполняют операцию. В тех случаях, когда степень уменьшения опухоли больше 50% её первоначального объема, а остаток небольшой, через 2 нед продолжают лучевую терапию до достижения терапевтической дозы (60-65 Гр). С помощью морфологических исследований было показано, что через 3-4 нед после предоперационной дозы лучевой терапии опухоль начинает восстанавливаться за счёт радиорезистентных клеток: тем самым нивелируется предоперационный эффект лучевой терапии. В связи с этим интервал между этапами лечения не должен превышать 2 нед.
Следует отметить, что хирургическое вмешательство, выполняемое после полной дозы лучевой терапии, чревато опасностью развития послеоперационных осложнений, приводящих к образованию свищей, аррозий магистральных сосудов, существенно пролонгирующих послеоперационный период и затрудняющих его ведение.
При лечении рака голосовых складок Т1-Т2 лучевую терапию проводят с двух встречных полей под углом 90°: высота поля составляет 8 см, ширина — 6 см. При наличии регионарных метастазов можно рекомендовать поля, направленные сзади наперёд под углом 110°.
Вместо методик классического фракционирования дозы (по 2 Гр 5 раз в неделю)
В настоящее время применяют более эффективную методику дробления дозы на 3,3 Гр (по 1,65 Гр с каждого поля) 3 раза а неделю. Используя эту методику, можно за 10 лечебных сеансов в течение 22 дней поднести к опухоли дозу 33 Гр, эквивалентную по эффективности 40 Гp. При продолжении лучевой терапии по радикальной программе на 2-м этапе подводят к опухоли еще 25Гр. При этом используют классическое фракционирование дозы по 2 Гр 5 раз в неделю как более щадящее. Это позволяет избежать повреждении хрящей и развития хондроперихондрита.
Помимо лучевой терапии, проводимой в обычных условиях (в воздухе), разработан метод лучевой терапии в условиях гипербарической оксигенации. Преимуществами этого метода при предоперационном облучении считают усиление лучевого повреждения опухоли, уменьшение лучевого повреждения нормальных тканей, включенных в объём облучения, снижение частоты лучевых эпителиитов.
Использование гипербарической оксигенации позволило снизить при предоперационном облучении суммарную очаговую дозу до 23,1 Гр (7 сеансов по 3,3 Гр>, что эквивалентно 30 Гр при классическом фракционировании в тех случаях, когда изначально планируют комбинированное лечение с выполнением резекции гортани. Морфологическое изучение лучевого патоморфоза показало, что III степень патоморфоза у этих больных была в 2 раза выше, чем после подведения 33 Гр в воздухе. Подобные наблюдения послужили основанием для расширения показаний к самостоятельной лучевой терапии в условиях гипербарической оксигенации по радикальной программе.
При раке вестибулярного отдела гортани Т1-Т2 лечение следует начинать с лучевой терапии. Верхнюю границу поля облучения поднимают выше горизонтальной ветви нижней челюсти на 1,5-2 см. Методика фракционирования дозы и уровень суммарных очаговых доз при предоперационной лучевой терапии и облучении по радикальной программе для всех отделов гортани идентичны. Если после лучевой терапии в предоперационной дозе (40 Гр) опухоль уменьшается незначително (менее чем на 50%), то выполняют горизонтальную резекцию гортани.
Лечение рака вестибулярного отдела гортани ТЗ-Т4 начинают с химиотерапии. После 2 курсов химиотерапии проводят лучевую терапию в предоперационной дозе.
Окончательную тактику лечения определяют после подведения к опухоли дозы облучения 40 Гр. Больному выполняют резекцию гортани, если остаточная опухоль имеет небольшие размеры, и ларингэктомию при больших размерах опухоли, локализующиеся в области передней комиссуры, подкомиссуральной области, гортанного желудочка, черпаловидного хряща обычно радиорезистентны. Обнаружение поражения этих отделов гортани считают веским аргументом и пользу операции.
При раке подголосового отдела гортани ТТ-Т2 лечение также начинают с лучевой терапии. Её результаты оценивают после предоперационной дозы облучения 40 Гр. При уменьшении опухоли менее чем на 50% выполняют хирургическое вмешательство.
Зоны регионарного метастазирования включают в поле облучения при пред- или послеоперационной лучевой терапии по поводу рака гортани.
Наличие трахеостомы не является препятствием к проведению лучевой терапии: её включают в поле облучения.
Химиотерапию проводят больным распространённым раком надголосового отдела гортани (поражение корня языка, гортаноглотки, мягких тканей шеи). При раке подголосового и голосового отделов гортани химиотерапия малоэффективна.
Неоадъювантная химиотерапии состоит из 2 идентичных курсов с перерывами в 1 день между ними. Каждый блок включает:
- 1-й день. Циспластин в дозе 75 мг/м 2 на фоне гипергидратации и форсированного диуреза.
- на 2-5-е сутки фторурацил в дозе 750 мг/м 2 .
При выявлении радиорезистентности рака среднего отдела Т1-Т2 на 2-м этапе лечения после предоперационной лучевой терапии в дозе 40 Гр (в воздухе) выполняют органосохраняющую операцию. При раке голосового отдела гортани, если опухоль не распространяется на переднюю комиссуру и черпаловидный хрящ, выполняют боковую резекцию гортани. Если опухоль распространяется на переднюю комиссуру, производят переднебоковую резекцию . Следует отметить, что хирургический метод (резекция гортани) в качестве самостоятельного даёт сопоставимые результаты. Однако в этом случае исключена возможность излечения больного без операции с помощью лучевой терапии, при которой можно сохранить хорошее качество голоса.
При раке среднего отдела гортани ТЗ-Т4 на 1-м этапе проводят химиолучевое или лучевое лечение, на заключительном-ларингэктомию. В последние годы разработаны методики органосохраняющих операций операций при раке ТЗ, однако их выполняют по строгим показаниям. Излечение рака ТЗ с помощью лучевой терапии возможно только у 5-20% больных.
Разработана методика резекции гортани при ТЗ с эндопротезированием.
- поражение с одной стороны с переходом на переднюю комиссуру и другую сторону более чем на 1/3 при сохранении черпаловидных хрящей;
- поражение трёх отделов гортани с одной стороны с инфильтрацией подголосового отдела, требующее резекции перстневидного хряща.
Во избежание рубцового сужения гортани её просвет формируют на трубчатом протезе, изготовленном на основе винилпирролидона и акрилатон, пропитанных антисептиком, или из медицинского силикона. Через 3-4 нед после фор мирования каркаса просвета резецированной гортани протез удаляют через рот.
При раковой опухоли подголосового отдела гортани ТЗ-Т4 предоперационную лучевую терапию не проводят, т.к. у больных выражен стеноз просвета гортани до начала лечения или велика опасность его развития в процессе лучевой терапии Лечение начинают с ларингэктомии с 5-6 кольцами трахеи. Лучевую терапию проводят в послеоперационном периоде.
Основным методом лечения рецидивов рака гортани считают хирургического вмешательство. В зависимости от степени распространения опухоли, формы роста, морфологической дифференцировки планируют объём операции (от резекции до ларингэктомии).
Превентивные операции (при отсутствии пальпируемых и определяемых при УЗИ метастазов) выполняют при глубоком эндофитном росте опухоли с разрушением хрящей гортани, при распространении опухолей на гортаноглотку, щитовидную железу и трахею.
При наличии регионарных метастазов выполняют фасциально-футлярное иссечение лимфатических узлов и клетчатки шеи. При прорастании опухоли во внутреннюю ярёмную вену или грудино-ключично-сосцевидную мышцу резецируют эти анатомические структуры (операция Крайля). При обнаружении у больного раком гортани единичных метастазов в лёгких и печени решают вопрос о возможности их удаления.
После проведённого консервативного и хирургического лечения больным необходимо тщательное регулярное и длительное наблюдение. Режим наблюдении и первые полгода — ежемесячно, во вторые полгода — через 1,5-2 мес; на 2-Й год — через 3-4 мес, на 3-5-й годы — через 4-6 мес.
Потеря голосовой функции после ларингэктомии — одна из частых причин отказа больных от этой операции. В настоящее время широкое распространение получил логопедический метод восстановления голосовой функции.
Однако метод имеет ряд недостатков: трудности с освоением методики заглатывания воздуха в пищевод и его выталкивания при фонации, небольшой пищевода (180-200 мл) в качестве резервуара для воздуха, гипертонии или спазм сжимателей глотки. При использовании этого метода хорошего качества голоса можно добиться у 44-60% пациентов.
Этих недостатков лишен существенно усовершенствованный хирургический метод реабилитации голоса после ларингэктомии. Он основан на принципах спадании шунта между трахеей и пищеводом, через который мощный поток воздуха из лёгких проникает в пищевод и глотку. Поток водуха вытыкает вибрационную активность глоточно-пищеводного сегмента, являющегося генератором голоса. Голосовой протез, помещённый в просвет шунта, пропускает воздух из лёгких в пищевод и препятствует попаданию жидкости и нищи в обратном направлении.
Проведённый акустический анализ выявил большие преимущества трахео-пищеводного голоса (с использованием голосовых протезов) перед пищеводным. С помощью этого метода хорошее качество голоса было достигнуто у 93,3% пациентов.
Таким образом, после операций по поводу рака гортани необходимо восстановление голосовой функции.
источник
Рак гортани – очень опасная патология, которая в начале своего развития не сопровождается какой-либо симптоматикой и в то же время быстро растёт. Страдают от неё в основном мужчины, что связано с их образом жизни. У женщин раковые опухоли в гортани диагностируют достаточно редко, что всё же не мешает некоторым представительницам прекрасного пола попасть в группу риска.
Данный недуг является злокачественным новообразованием, развивающимся в эпителиальных тканях данной анатомической части человеческого организма. В 95% клинических случаев диагностируют плоскоклеточный рак гортани .
Как и любая злокачественная опухоль, данное раковое новообразование имеет ряд особенностей, увеличивающих его опастностьдля жизни:
1. Чаще всего развивается у мужчин в возрасте, когда многие терапевтические мероприятия бывают недопустимы.
2. Активно разрастается и рано начинает метастазировать и этим значительно снижает шансы пациентов на излечение.
3. Растет только инфильтративно, т. е. преобразовавшиеся элементы прорастают близлежащие тканевые структуры и сливаются с ними, что сильно затрудняет проведение адекватную тотальную резекцию новообразования.
Что способно спровоцировать злокачественное перерождение клеток в гортанной области, до сих пор выяснено не до конца, но учёные называют ряд факторов риска, ускоряющих зарождение и развитие патологического процесса.
Основные причины рака гортани, по мнению специалистов, заключаются в следующем:
• наличие вредных привычек, курения и злоупотребления крепким алкоголем;
• длительный стаж работы в тяжёлой промышленности с выбросами в воздух химических веществ, металлической и древесной пыли;
• приверженность к употреблению острой и горячей пищи;
• произошедшие ранее механические повреждения горла.
Стоит знать! Все эти негативные факторы провоцируют термические, механические и химические повреждения слизистой гортанной области, что в свою очередь приводит к началу мутации составляющих её клеток. Помимо вышеуказанных причин стоит особо отметить ряд заболеваний: бронхогенный кисты, фиброму на широком основании, папилломы, хронические ларингиты и фарингиты . Эти патологии считаются предраковыми заболеваниями, способными под воздействием негативных факторов в короткие сроки переродиться в раковую опухоль.
Начальный этап развития патологического процесс, как уже говорилось, протекает скрытно, но всё-таки, при внимательном отношении к своему здоровью и самочувствию, человек может заподозрить зарождение опасного заболевания. Самый первый признак рака гортани – появление сухого кашля и осиплости голоса.
Кроме него специалисты советуют обращать внимание на следующие не специфические симптомы рака гортани:
• выраженное першение и дискомфорт в горле;
• ощущение при глотании постороннего предмета;
• неявная болезненность в гортанной области, усиливающаяся при совершении человеком глотательных движений.
Важно! Если появились и длительное время (больше 2 недель) не исчезают такие первые признаки рака гортани, способные сопровождать любое заболевание верхних дыхательных путей, необходима консультация специалиста. Только опытный врач сможет выяснить в чём их причина – онкологическом процессе в горле или банальном воспалении гортанной области.
Начиная с третьей стадии, симптомы рака горла становятся более выраженными. Но, несмотря на значительное прогрессирование онкологического процесса, больной может все еще не догадываться о наличии опухоли.
Находящийся на завершающем этапе и активно прогрессирующий рак гортани симптомы, признаки и основные визуальные проявления имеет очень яркие. К ним относятся:
• практически полная потеря аппетита и резкое похудение вплоть до явной кахексии;
• увеличение и затвердение шейных лимфоузлов, появление в них сильных болей;
• хронический сухой кашель со скудными выделениями кровянистой мокроты;
• острая болезненность при совершении глотательных движений;
• появление во рту неприятного привкуса и гнилостного аромата;
• выраженная охриплость или полная потеря голоса;
• затруднение проглатывания даже жидкой пищи.
Перечисленные симптомы рака горла и гортани возникают не одновременно. Они могут различаться в зависимости от размера и локализации опухолевой структуры, возрастной категории больного и наличия у него сопутствующих заболеваний. К примеру, если злокачественный очаг расположен в верхнем отделе горла, усиление болевого синдрома происходит во время совершения глотательных движений, а если непосредственно в центральной части, при произношении слов. На финальных стадиях патологического процесса симптомы рака гортани усиливаются проявлениями поражения органов, в которые проросли метастазы. Помимо этого появляется риск развития в поражённых участках сепсиса.
В зависимости от того, насколько выражены патологические изменения, произошедшие в слизистой, выделяют 4 стадии рака гортани.
Каждая из них характеризуется своими морфологическими признаками и клиническими симптомами:
1. Рак гортани на ранней стадии представляет собой объёмное, выступающее в просвет гортанной области, образование или небольшую язвочку и локализуется только в одном из отделов. Клинические признаки на этом этапе болезни полностью отсутствуют или имеют минимальную выраженность.
2. Рак гортани 2 степени характеризуется прорастанием опухолью полностью одного отдела, в котором она зародилась, но поражение 2 других пока отсутствует. Появляются характерные для этого заболевания признаки.
3. Рак гортани на 3 стадии злокачественное новообразование поражает соседний отдел или прорастает вглубь гортанных тканей, из-за чего нарушается подвижность данной анатомической области. Появляются первые метастазы в регионарных лимфоузлах и значительно усиливается клиническая симптоматика.
4. Рак гортани 4 стадии характеризуется разрастанием опухолевой структуры до гигантских размеров и поражением ей не только всей гортанной области и регионарных лимфоузлов, но и прорастанием в отдалённые органы. Сопутствующие патологическому процессу симптомы становятся невыносимыми, а болезнь переходит в категорию неизлечимых.
Благодаря многочисленным достижениям современной онкологии, данный недуг перестал быть окончательным смертным приговором для пациента. Основным условием успешного излечения является раннее обращение к специалисту.
Современное лечение рака гортани проводится с помощью следующих методов:
1. Лучевая терапия и брахиотерапия. Обычно проводится предоперационное облучение в течение недели. За это время суммарная доза радиации должна достигнуть 40 Гр. В случае выявления высокой степени радиочувствительности опухоли после двухнедельного перерыва продолжают облучение до СОД в 65-70 Гр. При недостаточной радиочувствительности пациенту назначается операция.
2. Хирургическое удаление рака гортани является золотым стандартом в лечении этого заболевания. Его проводят несколькими способами, отличающимися глубиной резекции органа – хордэктомия применяется когда необходимо удалить только одну голосовую складку, гемиларингэктомия подразумевает резекцию половины гортанной области, а при тотальной ларингэктомии вырезают весь орган полностью. После последней операции необходима пластическая хирургия – пациенту устанавливается трахеостома. При раке гортани после удаления она выполняет функции искусственного горла.
3. Таргетная терапия . Данный инновационный метод позволяет навсегда избавиться от опасного заболевания и при этом избежать опасных осложнений, т. к. данная процедура заключается во введении более мягкого, чем традиционные химиопрепараты, средства непосредственно в ткани горла.
4. Химиотерапия при раке гортани применяется достаточно редко, т. к. не имеет особой эффективности. В случаях назначения химии в протоколах комплексной терапии для тяжёлых онкобольных с неоперабельной опухолью используют следующую схему: Цисплатин в 1 день 80 мг/м2 + Гемцитабин 1250 мг/м2 инфузионно с 1 по 8 дни. Через 21 день цикл повторяют, а длительность курса лечения будет зависеть от общего состояния пациента, но не должна превышать 6 циклов.
С более подробной информацией, Вы можете ознакомиться на нашем сайте lor-24.ru .
источник
Рак гортани относится к опухолям визуальной локализации, что облегчает его диагностику и прогноз. При своевременном лечении до 80% пациентов переживают 5-летний рубеж. К сожалению, большинство случаев рака гортани диагностируется уже на распространенной стадии, хотя до появления регионарных метастазов прогноз остается сравнительно благоприятным. Подавляющее большинство злокачественных новообразований гортани приходится на плоскоклеточный рак.
Наибольшая заболеваемость раком гортани отмечается у мужчин в возрасте 40-60 лет, на которых приходится до 90% всех больных. При этом подавляющая часть является злостными курильщиками. Помимо этого факторами риска выступают:
- работы в условиях повышенной запыленности;
- хронические ларингиты;
- постоянный контакт дыхательных путей с канцерогенами — парами нефтепродуктов, фенола и других.
Отдельно следует отметить ВПЧ-ассоциированный рак, которому предшествует папилломатоз гортани, вызванный вирусом папилломы человека 16 и 18 подтипов.
Первые симптомы заболевания появляются относительно рано и зависят от локализации опухоли относительно голосовых связок: в надскладочном, подскладочном и складочном отделах.
Симптомы опухоли надскладочной локализации достаточно долго проявляются умеренно, и больной изначально не особо обращает на них внимание:
- сухость и першение в горле;
- боли при глотании;
- ощущение инородного тела в горле.
Подскладочный рак в большей степени характеризуется сужением дыхательных путей, что сопровождается инспираторной одышкой. Вместе с этим может отмечаться сухой кашель, что вкупе схоже с клинической картиной хронического ларингита.
При росте новообразования в области голосовых связок на первый план выходит нарастающая осиплость голоса, достигающая в дальнейшем полной афонии, когда человек полностью теряет возможность разговаривать в голос.
По мере роста опухоли, когда она распространяется за пределы гортани, к симптомам заболевания присоединяются гнилостный запах изо рта, кровохарканье, истощение, боли в горле, связанные с повреждением хряща и другое.
Стадирование новообразования осуществляется по общепринятой системе TNM, где T характеризует распространение первичного очага, N — поражение лимфатических узлов, а М — отдаленные метастазы. Обозначение “0” возле элемента означает отсутствие признака.
Рак in situ — скопление гистологически измененных клеток, не прорастающих в окружающие ткани.
Т1 — опухоль в пределах одной из анатомических областей: надсвязочной, подсвязочной или в области голосовых связок.
Т2 — прорастание за пределы анатомической области.
Т3 — дальнейший рост в пределах гортани с фиксацией голосовых связок или с повреждением щитовидного хряща.
N1 — метастазы в одном лимфоузле на стороне поражения с его увеличением до 3 см.
Т4а — новообразование прорастает хрящи гортани или распространяется на трахею, мягкие ткани, щитовидную железу, пищевод.
N2 — вовлечен либо один, либо несколько узлов со стороны поражения с ростом до 6 см.
Т4b — новообразование распространяется в средостение, оболочку сонной артерии, предпозвоночное пространство.
N3 — поражение лимфатических узлов с их увеличением более 6 см.
Заподозрить злокачественную опухоль гортани иногда возможно уже на этапе первичного приема при тщательной оценке жалоб и анамнеза, а также данных физикального исследования. Из методов инструментальной диагностики могут быть рекомендованы:
- Эндоскопическое исследование верхних дыхательных путей и органов пищеварения. Проводится всем пациентам с подозрением на рак гортани. При этом проводится также биопсия измененных участков слизистой оболочки для гистологического исследования.
- Ультразвуковое исследование шеи — для оценки регионарных лимфатических узлов, а также УЗИ брюшной полости для выявления отдаленных метастазов.
- Рентгенография — не самый достоверный, но очень доступный метод диагностики распространенности процесса в средостение или органы грудной клетки.
- ПЭТ-КТ — высокотехнологичное радиологическое исследование всего тела, позволяющее с максимальной точностью оценить распространенность опухолевого процесса.
- Компьютерная томография шеи и лицевого скелета с контрастированием — для оценки местной распространенности процесса.
- Остеосцинтиграфия — лучевой метод исследования костей, позволяющий выявить их поражение метастазами.
Всем без исключения пациентам показано гистологическое исследование тканей опухоли.
Основными направлениями лечения рака гортани традиционно являются хирургические, радиотерапевтические и химиотерапевтические методы. На начальных стадиях в качестве основного метода лечения рекомендуется проведение лучевой терапии, так как результаты лечения не уступают хирургическим вариантам, при этом сохраняется гортань и, как следствие, качество жизни. При более распространенных стадиях (Т3-Т4) в качестве радикального метода рекомендована операция, которая может быть дополнена адъювантной или неоадъювантной химиолучевой/лучевой терапией.
Адъювантная терапия — вспомогательное лечение, назначаемое после операции, неоадъювантная — перед ней.
Операция показана в большинстве случаев рака гортани. При этом в зависимости от стадии и распространенности опухоли, это может быть как полное удаление гортани (ларингэктомия), так и частичное — иссечение новообразования в пределах здоровых тканей (резекция гортани). Последнее может быть выполнено в ходе открытой или эндоскопической операции.
Возможно независимое применение лучевой терапии вместо операции.
Опухоли Т1 и Т2, возможно с N1
Возможна резекция гортани или лучевое лечение с удалением пораженного лимфоузла.
Ларингэктомия в большинстве случаев с удалением вовлеченных лимфоузлов или химиолучевая терапия.
Тотальная ларингэктомия или конкурентная химиолучевая терапия.
Тотальная ларингэктомия с адъювантной химиолучевой терапией. При отказе от операции — химиолучевая терапия.
Приведенная информация лишь ориентировочно дает представление о возможной тактике врачей. В каждом клиническом случае специалисты решают этот вопрос, отталкиваясь от целого ряда факторов, например, технической возможности полностью удалить опухоль.
Классическая лучевая терапия выполняется обычно в трех вариантах:
- Самостоятельная лучевая терапия может быть направлена как на первичный очаг, так и на регионарные метастазы. Является альтернативой хирургическому лечению. Длительность лечения при этом составляет 6-7 недель.
- Конкурентная химиолучевая терапия проводится при более распространенном процессе и представляет собой одновременное использование химиотерапевтических препаратов и дистанционное излучение.
- Адъювантная лучевая терапия назначается после операции. Она может быть назначена, например, когда по каким-либо причинам не получилось добиться чистых краев резекции — опухоль была удалена не полностью. Так же после операции в ряде случаев показано проведение конкуррентной химиолучевой терапии.
В целом, применение химиолучевой терапии обусловлено стремлением сохранить гортань.
| Наименование услуги | Цена, руб. | Ед. измерения |
|---|---|---|
| Консультация врача онколога радиотерапевта | 1 500 | шт. |
| Консультация врача детского онколога | 1 500 | шт. |
| Повторная консультация специалистов | 500 | шт. |
| Топометрия на специализированном компьютерном томографе первичная | 15 000 | процедура |
| Топометрия на специализированном компьютерном томографе повторная | 7 000 | процедура |
| Дозиметрическое планирование лучевой терапии (томотерапии) первичное | 20 000 | шт. |
| Дозиметрическое планирование лучевой терапии (томотерапии) повторное | 7 000 | шт. |
| Лучевая терапия (томотерапия), включая IMGRT (*) | 223 000 | курс |
| Лучевая терапия (томотерапия) стереотаксическая радиохирургия(*) | 250 000 | курс |
| Лекарственная сопроводительная терапия: внутривенные введение в процедурном кабинете (без учета стоимости лекарственных препаратов) | 1 000 | процедура |
| Лекарственная сопроводительная терапия: внутримышечное введение в процедурном кабинете (без учета стоимости лекарственных препаратов) | 200 | процедура |
| Топометрическая разметка | 750 | процедура |
Вид лучевой терапии и количество сеансов курса определяется врачебной комиссией индивидуально для каждого пациента исходя из локализации, нозологии опухоли и с учетом анамнеза.
Химиотерапия — воздействие на злокачественные клетки лекарственными препаратами, а чаще их комбинациями. При раке гортани применяется обычно в следующих режимах:
- Индукционная химиотерапия — курс лечения, задачей которого стоит добиться ремиссии заболевания, то есть приостановить его прогрессирование. Применяется в виде комбинации лекарственных препаратов перед курсом химиолучевой терапии.
- Как компонент конкурентной химиолучевой терапии. Термин “конкурентная” здесь означает, что оба компонента курса назначаются одновременно, а не последовательно
Самостоятельно химиотерапия назначается при неоперабельных опухолях и отдаленных метастазах. Количество курсов во многом зависит от эффективности лечения.
Принципиально новые возможности в органосохраняющем лечении открывает лучевая терапия с модулированной интенсивностью, и в частности технология TomoTherapy.
Томотерапия — система, которая совмещает в себе линейный ускоритель электронов и компьютерный томограф, что позволяет четко локализовать опухоль и направить на нее поток ионизирующего облучения, минимально затрагивая здоровые ткани. Таким образом удается улучшить переносимость лучевой терапии и повысить качество жизни пациентов после проведенного лечения.
источник
Одним из применяемых способ лечения рака гортани является лучевая терапия. Используя метод, удаётся излечить онкологию на ранних этапах развития и остановить метастазы в органы и лимфоузлы. Лечение происходит ионизирующим облучением.
Самыми используемыми в онкологии при лечении радиотерапии считаются два направления – внешнее облучение и брахитерапия (внутреннее).
Процедура происходит с размещением в поражённом органе радиоактивных заряженных частиц. Таким образом, возникает разрушение злокачественной опухоли. Лечение проводится аппаратом или вручную. При применении этого метода можно обойтись без удаления органа.
Проводится терапия после обследования пациента. В список исследований входит УЗИ, КТ, МРТ, ЭКГ. Затем врачи (онколог, хирург, радиолог) высчитывают количество радиоактивного препарата. Капсулы создаются индивидуально. Назначается диета из продуктов, не вызывающих метеоризм, перед процедурой ставится клизма.
Продолжительность около часа. Проводится с анестезией, так как метод болезненный. Капсулы вживаются в ткань поражённой области тонкими иглами аппаратным или ручным способом. Их расположение зависит от опухолевой формы, окружающих клеток. На экран выводится процесс размещения капсул. Они могут присутствовать в теле больного временно либо оставаться на всю жизнь. Важна грамотно рассчитанная доза вещества.
К достоинствам процедуры относится быстрая реабилитация и нахождение в стационаре, небольшой список осложнений и побочных проявлений, малая кровопотеря, снижение рецидива.
Это наружная радиотерапия. Находит применение для лечения при раке гортани, головного мозга, лёгких, предстательной и молочной желёз. Перед лечением проводится диагностическое обследование. Врачи рассчитывают дозу и угол воздействия излучения, чтобы точно попасть на опухоль. Онколог выделяет границы злокачественной опухоли, чтобы в процессе облучения не задеть здоровые участки.
Пациент размещается в специальной камере. Точное расположение человека определяется с применением рентгена, УЗИ, КТ. Затем ионизирующий луч направляется на шею. Продолжительность воздействия на участок составляет несколько минут. Процедура безболезненная.
Выборочное облучение гортани позволяет не затрагивать лимфоузлы, оказывает минимальное воздействие слюнных желёз, ротовой полости, нижней челюсти, ротоглотки.
Длительность курса излучения составляет более шести недель. На второй стадии, с нарушением движения голосовой складки, улучшению контроля над развитием опухолевой ткани помогает дробление доз облучения неоднократно в день. Тогда повышается токсичность. На этом этапе может понадобиться селективное излучение лимфатических узлов шеи.
Химиотерапия совместно с лучевым воздействием применяется на третьей стадии рака. Также используется для предотвращения повторного онкологического заболевания, особенно если был использован хирургический метод устранения опухоли. На четвёртом этапе онкологии, когда опухолевый узел крупных размеров и операция не проводится, лучевое воздействие и химиотерапия являются главным способом лечения.
При наличии раковых метастазов излучение проводится для снижения боли, давления на участке опухоли. Это облегчает состояние пациента, такой метод носит название паллиативной лучевой терапией.
Для лечения расширенного рака голосового аппарата применяют ларингоэктомию – это операция по удалению гортани. Данный хирургический метод используют при раке горла 3-4 степени, когда опухоль прорастает в ближайшие ткани. Ларингоэктомия бывает тотальная (поражённая гортань удаляется полностью) и частичная (удаляется часть гортани, к примеру, голосовая связка). После операции проводят лучевую терапию.
Даже при хорошей чувствительности опухоли на ионизированное облучение, имеются противопоказание для лечения. Основными показаниями к запрету для радиоактивного излучения считаются:
- Наличие хронических болезней дыхательной, мочевыводящей, сердечно-сосудистой, нервной систем. Проведение лечения ухудшает состояние, приводит к осложнениям.
- Разрастание злокачественной опухоли в сосуды кровеносной системы, пищевод и лимфоузлы.
- Истощение организма.
- Изменения в кровяной структуре, анемия.
- Злокачественный узел распадается, возможны кровотечения.
- Инфекционные и воспалительные процессы, с присутствием лихорадки и высокой температуры тела. При лечении может возникнуть новая опухоль.
Терапия излучением приводит к побочным проявлениям. Как они проявятся, зависит от длительности лечения и дозы облучения. При проведении вместе с химиотерапией неблагоприятные последствия могут усилиться.
Развитие побочных эффектов происходит по истечению 14 дней после радиотерапии. В ближайшую неделю после того, как закончилась лучевая терапия, усиливаются проявления. Постепенно состояние нормализуется.
Перед началом процедуры медицинский специалист проконсультирует о возможных побочных симптомах, расскажет, как их контролировать.
К указанным симптомам относятся:
- Ощущение усталости. Характерно для окончания терапии. Нужен постоянный отдых, небольшая физическая активность – благоприятно сказываются пешие прогулки на короткие дистанции.
- Кожные изменения. Кожные покровы на передней области шеи со временем обретают красный или тёмный цвет. У смуглого пациента кожа синеет или чернеет. Иногда возникает зудящий, болевой синдром. Перемены характерны через 14 дней после терапии при раке гортани и длятся в течение месяца после окончания. Медицинский работник (медсестра или врач-рентгенолог) даст рекомендации по уходу за кожными покровами в месте обработки излучением. Сюда относятся следующие принципы:
- Поддержание чистоты, аккуратное мытьё водой комфортной температуры и мылом без ароматических добавок. Вытирать мягким полотенцем.
- Не применять духи, туалетную воду на участке обработки, чтобы избежать раздражающих проявлений.
- В душе пользоваться слабым водным напором. Для увлажнения применять крема без запаха.
- Противопоказаны воротники с жесткой основой, одежда должна быть свободной, из хлопковых тканей. Для пребывания на улице шею закрывают от солнечных лучей, холодного ветра.
- Врач может назначить крем, если наблюдается шелушение, трещины, воспаления. Возможно, потребуется наложение стерильной повязки.
- Наличие боли в гортани, сложно глотать. Возникает из-за поражения слизистой поверхности воспалением. Чтобы облегчить болевой синдром, назначаются обезболивающие в жидком виде. Медицинские специалисты посоветуют потреблять продукты, которые легко проглотить. Также показано к употреблению питательное, с высоким содержанием калорий питье. Многие больные кушают размягчённую и влажную еду. Болезненность горла исчезает через несколько недель после облучения.
Формирование данного симптома может привести к истощению человека, из-за невозможности потреблять достаточный объём пищи. Такой показатель характерен для совмещения лучевой и химической терапии. Для этого случая доктор советует искусственное поступление еды, для поддержания массы тела. Также поступают медикаменты и жидкость. Искусственное питание позволяет контролировать вес, предоставляет нужное количество воды, снижает давление. Для осуществления поступления пищи в организм используют тонкую трубку, которая проходит через нос или делается отверстие в коже. Такое питание позволяет не прекращать терапию из-за снижения веса.
- Ощущение сухости в ротовой полости либо гортани. Облучение оказывает воздействие на выработку слюнной жидкости. Снижение слюны приводит к сухости. Возникают сложности с речью и потреблением еды. Желательно частое потребление воды, очищение полости рта два раза в день. Такой эффект наблюдается после окончания излучения на протяжении месяцев.
- Загустение слюны, наблюдается липкость. Требуется постоянное полоскание, сплёвывание образовавшейся слизи.
- Голосовые изменения. Во время терапевтического вмешательства имеется риск преобразования голоса. Врач порекомендует не посещать задымленные места и регулярный покой голосовому аппарату.
- Снижение аппетита. Происходит из-за того, что больной не чувствует вкус еды при наличии болезненности в горле. Такие симптомы характерны окончанию терапевтического метода. Диетолог назначит питательные напитки, которые потребляются до тех пор, пока желание кушать не восстановится.
- Потеря вкусового восприятия.
- Наблюдается выпадение волосяного покрова на лице.
- Трудности с дыханием. Облучение может привести к возникновению отёка в горле. Требуется медицинская помощь, иногда прибегают к хирургическому вмешательству.
Эффективность лечения лучевой терапией зависит от стадии развития болезни. Учитывается место возникновение новообразования, объём и степень поражения, восприимчивость к радиоактивному лечению. Опасным последствием считается злокачественный процесс, который наблюдается при плоскоклеточном раке горла. Заболевание обладает признаками простудных болезней, что приводит к позднему посещению врача и невысокими шансами на излечение.
Начальная стадия рака гортани даёт высокий шанс излечить болезнь. Лучевая терапия поможет избежать повторного формирования злокачественной опухоли, но полностью стволовая клетка рака не исчезнет. Не стоит забывать про перечень возможных осложнений.
источник
а) Лучевая терапия складочного отдела гортани. Новообразования голосовых складок ранних стадий имеют низкую метастатическую активность, поэтому зачастую они могут быть успешно устранены использованием лишь одного метода лечения. На ранних стадиях применяется либо хирургическое, либо лучевое лечение; распространенные формы рака требуют комбинации хирургического, лучевого и химиотерапевтического воздействия.
При распространенных опухолях мультидисциплинарный подход позволяет достичь максимального излечения, сохранить функцию пораженного органа, ограничить регионарное распространение, а также гораздо проще приспособиться к сопутствующим заболеваниями пациента и его индивидуальным предпочтениям.
На ранних стадиях заболевания при помощи лучевой терапии без ее сочетания с химиотерапией можно добиться и контроля опухолевого роста, и сохранения функции гортани. На настоящий момент чаще всего используются простые односторонние латеральные поля излучения в дозе 63-65 Гр за 28-29 сеансов в течение пяти с половиной недель.
Избирательное облучение гортани, не затрагивающее регионарные лимфоузлы, позволяет минимизировать повреждение крупных слюнных желез, нижней челюсти, ротоглотки и полости рта. Важны длительность курса и общая доза облучения. Оптимальная продолжительность курса составляет менее шести недель. У пациентов с опухолью стадии Т2 и с нарушением подвижности голосовой складки улучшить контроль над местным ростом опухолевой ткани можно посредством гиперфракционированного облучения (однако возрастает и общая токсичность).
Опухоли стадии Т2, поражающие надскладочный отдел гортани, могут потребовать селективного воздействия на лимфоузлы шеи. Подавления опухолевого роста можно добиться более чем в 90% случаев на стадии Т1, и более чем в 80% на стадии Т2.
При распространенном раке гортани стандартом лечения остается тотальная ларингэктомия с последующей лучевой терапией. Министерством по делам ветеранов США было организовано исследование эффективности лечения больных с раком гортани (Department of Veterans Affairs (VA) Laryngeal Cancer Study). Согласно его результатам, добиться сохранения функции гортани удалось у 2/3 пациентов, которым проводилась индукционная терапия тремя курсами 5-фторурацила/цисплатина с последующей лучевой терапией.
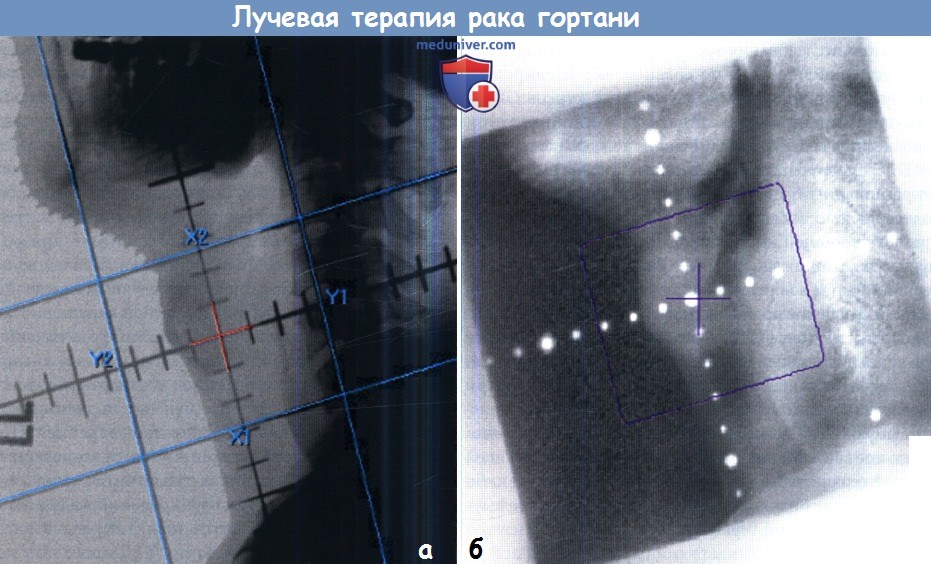
Двухмерная техника с использованием противоположных латеральных полей. Верхняя и нижняя границы устанавливаются с учетом подвижности гортани, которая будет отмечаться во время лечения.
Обратите внимание на то, что лимфоузлы не облучаются.
В качестве контрольной группы были выбраны пациенты, которым выполнялась тотальная ларингэктомия с последующей послеоперационной лучевой терапией. Разницы в выживаемости между двумя группами получено не было. Последующее крупное рандомизированное международное исследование сравнило курс лечения министерства по делам ветеранов (VA) с химиолучевой терапией и с изолированной лучевой терапией. Согласно его результатам, химиолучевая терапия позволяет добиться большей вероятности сохранения гортани, чем курс министерства (с 75% до 88%), поэтому на данный момент химиолучевая терапия является стандартом лечения.
Статистически значимой разницы в выживаемости между тремя группами получено не было (из-за высокой частоты выполнения ларингэктомий в качестве «терапии отчаяния»).
Следовательно, для пациентов с хорошим функциональным статусом гортани рекомендуется проведение семинедельной лучевой терапии с общей дозой в 70 Гр в сочетании с тремя курсами цисплатина в высоких дозах (100 мг/м 2 ). В качестве альтернативы может использоваться индукционная трехкомпонентная (TPF) химиотерапия с последующей лучевой терапией, данная схема также позволяет добиваться высокой частоты сохранения гортани. Две эти схемы лечения рака гортани не сравнивались в рандомизированных исследованиях.
У ослабленных пациентов, которые не могут перенести стандартный курс химиотерапии, может использоваться либо изолированная лучевая терапия, либо лучевая терапия в сочетании с биологической терапией (моноклональные антитела против ЭФР).
У пациентов, получающих изолированную лучевую терапию, можно использовать либо курс модифицированного фракционного облучения (либо с гиперфракционированием, либо ускоренным курсом), поскольку превосходство двух этих схем над стандартной однодневной схемой облучения была продемонстрирована в исследовании RTOG 90-03.
Из названных выше исследований исключались пациенты, у которых опухоль прорастала в хрящи гортани и/или окружающие мягкие ткани. В данной группе стандартом лечения является ларингэктомия с последующей адъювантной лучевой терапией и, возможно, химиотерапией.
б) Лучевая терапия надскладочного отдела гортани. Пациенты с опухолями надскладочного отдела нуждаются в терапии лимфоузлов шеи даже на ранних стадиях заболевания, поскольку риск их вовлечения крайне высок. Первичная опухоль может распространяться в окологортанное пространство, вызывая фиксацию голосовых складок; в преднадгортанное пространство с поражением корня языка; через щитовидный хрящ проникать в мягкие ткани шеи; при латеральном распространении возможно поражение горганоглотки.
Опухоли Т1/Т2 надскладочного отдела требуют лечения первичного очага и лимфатических узлов уровней II—IV. Как и при раннем раке голосовых складок, в данном случае можно использовать какой-то один метод лечения. При лучевой терапии используют дозу 66-70 Гр для первичного очага и 50-54 Гр для элективного лечения лимфоузлов шеи. При использовании традиционных схем возможно избежать облучения околоушных слюнных желез и верхнего констриктора глотки.
При распространенных опухолях у пациентов с исходным хорошим функциональным статусом гортани и удовлетворительным общим состоянием используется химиолучевая терапия. При значительном нарушении функции гортани и/или распространении опухоли за пределы органа прибегают к ларингэктомии с последующей адъювантной лучевой терапией.
в) Лучевая терапия подскладочного отдела гортани. Опухоли, расположенные под голосовыми складками, встречаются крайне редко. Визуализировать их сложно даже с использованием эндоскопического оборудования, часто для этого требуется общая анестезия. Из-за своего скрытого расположения данные новообразования часто диагностируются уже на поздних стадиях, когда опухоль распространяется в трахею и мягкие ткани шеи.
Они способны метастазировать в нижние шейные лимфоузлы и верхние лимфоузлы средостения. Комбинированное хирургическое лечение показано при опухолях Т4 стадии, в остальных случаях прибегают к лучевой терапии, захватывающей и первичный очаг опухоли, и пути лимфатического оттока.
источник
Под словосочетанием «рак горла» подразумевают, как правило, злокачественные опухоли гортани — органа, который участвует в проведении воздуха и формировании голоса. Эти опухоли относят к более обширной группе рака головы и шеи.
Верхний край гортани начинается возле корня языка, нижний переходит в трахею. По форме ее можно сравнить с воронкой, направленной узкой частью вниз. Ее стенки состоят из хрящей, мышц и связок, изнутри поверхность выстлана слизистой оболочкой. В гортани различают три отдела:
- Верхний отдел находится над голосовыми связками.
- Средний отдел включает голосовые связки.
- Нижний отдел расположен под голосовыми связками.
Некоторые цифры и факты, касающиеся рака гортани:
- Две основные причины заболевания — курение и употребление алкоголем. Табачный дым и этиловый спирт обладают канцерогенным действием, они вызывают мутации в клетках слизистой оболочки и их злокачественное перерождение.
- В последние годы распространенность заболевания снижается на 2–3% ежегодно. Отмечается прямая корреляция с уменьшением распространения курения.
- Около 60% злокачественных опухолей гортани развиваются в области голосовых связок. Еще 35% приходятся на верхний отдел, остальные случаи — на нижний, либо когда опухоль захватывает более одного отдела.
Практически все злокачественные опухоли гортани — это плоскоклеточный рак, который развивается из клеток слизистой оболочки. Нередко этому предшествуют предраковые изменения. Зачастую дисплазия не трансформируется в рак и исчезает самостоятельно, особенно если устранены повреждающие факторы — например, человек бросил курить.
В некоторых случаях предраковые изменения трансформируются в «рак на месте» — in situ. Он не прорастает за пределы слизистой оболочки, при раннем обнаружении успешно поддается лечению. Рак in situ — это опухоль нулевой стадии. Если ее не лечить, в дальнейшем она прогрессирует. Градация на стадии различается в зависимости от того, в каком отделе органа находится злокачественная опухоль. В таблице в общих чертах приведена классификация по стадиям:
Над голосовыми связками: опухоль находится в пределах верхней части гортани, не распространяется на другие отделы и не нарушает работу голосовых связок. Не поражены регионарные лимфатические узлы, нет отдаленных метастазов.
В области голосовых связок: опухоль проросла глубже по сравнению с раком in situ, но не нарушает подвижность голосовых связок. Нет отделанных метастазов, не поражены лимфатические узлы.
Под голосовыми связками: опухоль находится в пределах нижнего этажа гортани, не распространяется в лимфатические узлы и не дает отдаленных метастазов.
Над голосовыми связками: опухоль распространилась более чем на один отдел гортани, но все еще не нарушает движения голосовых связок.
В области голосовых связок: опухоль распространяется более чем на один отдел гортани и/или нарушена подвижность голосовых связок.
Под голосовыми связками: опухоль распространяется более чем на один отдел гортани, может нарушать подвижность голосовых связок.
Над голосовыми связками: опухоль нарушает подвижность голосовых связок и/или прорастает в окружающие ткани.
В области голосовых связок, под голосовыми связками: опухоль нарушает подвижность голосовых связок, или распространяется в окружающие ткани, или имеется один очаг размерами менее 3 см в регионарных лимфатических узлах.
Над, под и в области голосовых связок: опухоль сильнее распространяется в окружающие ткани, регионарные лимфатические узлы, имеются отдаленные метастазы.
Помимо плоскоклеточного рака, в гортани встречаются аденокарциномы. Они обнаруживаются очень редко, но в последние 20 лет, по данным статистики Великобритании, их распространенность растет.
Основные два фактора риска рака гортани — это курение и употребление алкоголя. При этом риски прямо пропорциональны силе вредных привычек:
- У людей, которые пьют много спиртного, риск повышен примерно втрое.
- У человека, который выкуривал по 25 сигарет ежедневно в течение 40 лет и более, риск повышен в 40 раз.
- Если человек одновременно курит и злоупотребляет алкоголем, его вероятность заболеть еще выше.
Другие факторы риска рака гортани:
- Возраст. Заболевание очень редко встречается среди людей младше 40 лет.
- Папилломавирусная инфекция. Исследования показали, что в развитии злокачественных опухолей гортани играет роль вирус папилломы человека 16 типа. Но этот вопрос требует дальнейшего изучения.
- Особенности питания. Рацион, который содержит мало витаминов и минералов, много обработанного красного мяса.
- Семейная история. Риск повышен у людей, у которых в семье были случаи диагностированного рака головы и шеи.
- Снижение иммунитета. ВИЧ/СПИД повышает риск примерно в 3 раза, препараты для подавления иммунитета после трансплантации органов — в 2 раза.
- Воздействие некоторых вредных веществ: формальдегида, древесной и угольной пыли, сажи, красок, дыма от сгорания угля.
- Гастроэзофагеальный рефлюкс. Кислый желудочный сок может повреждать слизистую оболочку пищевода и гортани, вызывать в них изменения, способствующие развитию рака.
- Генетические дефекты. Рак гортани иногда развивается у детей, которые не имеют ни одного фактора риска. Предположительно это происходит из-за некого неизвестного дефектного гена.
Нужно понимать, что «причина» и «фактор риска» — не одно и то же. Наличие факторов риска еще не гарантирует того, что у человека обязательно будет диагностировано онкологическое заболевание. Каждый из них лишь в определенной степени повышает вероятность.
Симптомы и проявления опухоли гортани могут быть разными, в зависимости от того, какой отдел органа поражен. Если образование локализовано в надсвязочном отделе, то на ранних стадиях больной будет жаловаться на:
- Дискомфорт при глотании.
- Чувство инородного тела.
По мере роста опухоли, к данным симптомам присоединяются:
- Нарастающая боль в горле, которая может иррадиировать в околоушную область.
- Значительное снижение массы тела. Пациент ограничивает себя в пище из-за наличия вышеперечисленных симптомов рака гортани, вследствие чего стремительно худеет.
- В результате опухолевой инфильтрации может развиться ригидность надгортанника. При этом состоянии в процессе глотания просвет гортани не закрывается полностью, что приводит к дисфагии и сильному кашлю по причине попадания пищи в трахею.
Опухоли связочного отдела являются наиболее прогностически благоприятными, так как их проявления даже на ранних стадиях доставляют больному выраженный дискомфорт и, как правило, заставляют обратиться к врачу.
Симптомы рака голосовых связок:
- Охриплость.
- Затруднение дыхания (характерно для поздних стадий, развивается при увеличении опухоли).
При локализации новообразования в подсвязочном отделе симптомы рака горла схожи с поражением голосовых связок: наблюдается охриплость, иногда может затрудняться дыхание на вдохе. Однако данный тип проявляет себя клинически на более поздних стадиях.
Опухоли подсвязочного отдела встречаются редко: всего в 2% случаев. У 23% больных выявляется одновременное поражение двух или всех трех отделов гортани.
Во время первичного приема врач расспрашивает пациента о симптомах, образе жизни, вредных привычках, осматривает и ощупывает шею. Прямо в кабинете может быть проведена непрямая ларингоскопия: врач просит пациента открыть рот и осматривает гортань с помощью небольшого зеркальца, введенного через рот.
При подозрении на онкологическое заболевание в первую очередь назначают прямую ларингоскопию (осмотр гортани с помощи специальных инструментов — гибкого фиброскопа или жесткого ларингоскопа), эндоскопическое исследование трахеи, пищевода, бронхов. Во время этих исследований можно провести биопсию: обнаружив патологически измененный участок слизистой оболочки, удаляют его фрагмент и отправляют в лабораторию для цитологического, гистологического исследования.
Биопсия позволяет с высокой точностью диагностировать злокачественную опухоль. Но на этом обследование зачастую не заканчивается. Нужно оценить, насколько сильно опухоль проросла в стенку гортани и окружающие ткани, есть ли поражение лимфоузлов, отдаленные метастазы. В этом помогают такие методы диагностики, как КТ, МРТ, ПЭТ-сканирование, сцинтиграфия костей, рентгенография желудка и пищевода с контрастированием сульфатом бария.
Тактика лечения зависит от расположения, размеров, стадии опухоли, от степени вовлечения окружающих тканей, лимфатических узлов, наличия отдаленных метастазов. Имеют значение и другие факторы: общее состояние здоровья, возраст пациента, сопутствующие заболевания.
Хирургия — основной метод лечения рака гортани. На ранних стадиях она может применяться самостоятельно, на более поздних — в сочетании с химиотерапией, лучевой терапией.
На ранних стадиях можно прибегнуть к эндоскопическому вмешательству (оно напоминает ларингоскопию), кордэктомии (удалению голосовых связок). Поверхностный рак можно удалить с помощью лазера, но такое вмешательство имеет недостаток: после него не остается фрагмента ткани для биопсии.
Также I-II стадии рака горла лечится при помощи проведения органосохраняющей резекции гортани, гемиларингэктомии. Для того чтобы предупредить развитие стеноза гортани в послеоперационном периоде, используется специальный расширяющий эндопротез, который удаляется спустя 3-4 недели.
В более запущенных случаях прибегают к ларингэктомии — полному или частичному удалению гортани. Она бывает разных видов:
- Частичная ларингэктомия — удаление части гортани, в которой находится опухоль.
- Верхнегортанная ларингэктомия — удаление верхнего отдела гортани.
- Гемиларингэктомия — удаление половины гортани.
- Тотальная ларингэктомия — удаление полностью всей гортани. При этом верхний конец трахеи подшивают к коже и формируют отверстие — такая операция называется трахеостомией. Через получившееся отверстие — трахеостому — пациент может дышать.
Часто пациенты интересуются: лечится ли рак горла с метастазами? При регионарном метастазировании во время проведения ларингэктомии хирурги иссекают шейную клетчатку и лимфатические узлы. Кроме того, при необходимости проводится резекция и других анатомических образований и органов шеи, если они вовлечены в опухолевый процесс (грудино-ключично-сосцевидная мышца, внутренняя яремная вена, глотка, щитовидная железа).
По показаниям после основного хирургического вмешательства выполняют реконструктивно-пластические операции. Если опухоль неоперабельна, но блокирует дыхательные пути, выполняют паллиативную трахеостомию.
При раке гортани часто приходится прибегать к лучевой терапии, причем, облучение может быть назначено с разными целями:
- В качестве адъювантного лечения после хирургического вмешательства, чтобы уничтожить оставшиеся раковые клетки, которые в будущем могут стать причиной рецидива.
- Для лечения рецидивировавшего рака.
- В качестве самостоятельного лечения при неоперабельных опухолях.
- Для борьбы с болью, кровотечением, нарушением глотания и костными метастазами на поздних стадиях.
- Самостоятельно на ранних стадиях рака. Некоторые небольшие опухоли можно уничтожить с помощью облучения, не прибегая к хирургическому вмешательству.
Рак горла лечится с применением обычного режима лучевой терапии или в сочетании с гипербарической оксигенацией. С помощью этого приема достигается увеличение повреждающего эффекта для клеток опухоли и уменьшается вред воздействия данного метода на окружающие здоровые ткани.
При злокачественных опухолях гортани применяют разные химиопрепараты: карбоплатин, цисплатин, доцетаксел, 5-фторурацил, эпирубицин, паклитаксел. Цели химиотерапии, как и лучевой терапии, бывают разными:
- Перед хирургическим вмешательством (неоадъювантная химиотерапия), чтобы уменьшить размеры опухоли.
- В сочетании с лучевой терапией (химиолучевая терапия) после операции для предотвращения рецидива.
- В составе химиолучевой терапии при неоперабельных опухолях на поздних стадиях.
- Для борьбы с симптомами при запущенном раке.
С применения химиотерапевтических препаратов всегда начинается лечение рака гортани III-IV стадии при локализации в среднем отделе. Опухоли, которые расположены в над- и подсвязочном отделе, этому виду лечения поддаются плохо.
Зачастую на поверхности опухолевых клеток при раке гортани находится большое количество белка-рецептора EGFR. Активируясь, он стимулирует деление клеток. В таких случаях эффективен таргетный препарат под названием цетуксимаб. Обычно его вводят внутривенно раз в неделю:
- На ранних стадиях в некоторых случаях цетуксимаб применяют в сочетании с лучевой терапией.
- На более поздних стадиях препарат назначают в комбинации с химиопрепаратами, в частности, с цисплатином, 5-фторурацилом.
Можно ли вылечить рак горла? При раннем выявлении опухоли процент излечения очень высок: при условии правильного лечения выздоровление наступает в 85-95% случаев. Возможности современной медицины позволяют помочь пациентам даже с поздними стадиями рака. В 5-20% больные с III стадией поражения среднего отдела гортани при грамотном подходе специалистов могут полностью выздороветь.
Лечение рака гортани может приводить к некоторым проблемам с питанием: нарушению глотания, снижению вкуса. После курса лучевой терапии беспокоят сильные боли, которые мешают глотать, нормально принимать пищу. Для борьбы с этим симптомом назначают обезболивающие препараты, кормление в течение некоторого времени может осуществляться через зонд. В дальнейшем противопоказаны продукты, которые приводят к раздражению горла.
После операции кормление осуществляется через назогастральный зонд или через гастростому — отверстие (как правило, временное), которое соединяет желудок с поверхностью кожи. Постепенно пациент может перейти на самостоятельный прием пищи.
Проблема, с которой сталкиваются многие больные — снижение чувства вкуса. Вкус пищи кажется недостаточно насыщенным, она как будто стала пресной. С этой проблемой помогают справиться специи, маринады, соусы.
Никакие методы народной медицины не могут эффективно бороться с какими то ни было онкологическими заболеваниями, включая рак гортани. Некоторые народные средства, фитопрепараты, БАДы помогают улучшить состояние и уменьшить симптомы, но другие могут повлиять на эффективность препаратов, ухудшить исход. Если вы решили использовать какие-либо средства альтернативной медицины, об этом, как минимум, нужно сообщить лечащему врачу.
На прогноз при раке гортани влияют разные факторы, но в первую очередь имеет значение стадия опухоли и ее расположение. В таблице ниже представлены средние показатели пятилетней выживаемости (процент пациентов, которые остаются в живых в течение 5 лет с момента диагностики рака):
Опухоли в верхнем отделе гортани:
- I стадия: 59%
- II стадия: 59%
- III стадия: 53%
- IV стадия: 34%
Опухоли в области голосовых связок:
- I стадия: 90%
- II стадия: 74%
- III стадия: 56%
- IV стадия: 44%
Опухоли в нижнем отделе гортани:
- I стадия: 53–65%
- II стадия: 39–56%
- III стадия: 36–47%
- IV стадия: 24–32%
На главные факторы риска рака гортани можно повлиять. Вот три основные рекомендации:
- Откажитесь от курения и вообще от употребления табака в любой форме. Опасны не только сигареты, но и трубки, сигары, кальяны, жевательный табак.
- Старайтесь употреблять как можно меньше алкоголя, желательно отказаться от него совсем.
- Меньше красного мяса и колбас, больше овощей, фруктов. Рацион должен содержать все необходимые витамины, минералы.
Риски можно снизить, но защититься на 100% не получится. Поэтому для людей, у которых повышен риск онкологических заболеваний, важно регулярно проходить скрининг. Однако, для рака гортани нет рекомендованных скрининговых программ. Этот тип рака встречается не так часто и нередко уже на ранних стадиях приводит к возникновению симптомов, поэтому массовый скрининг считается нецелесообразным.
Стоимость лечения рака гортани зависит от объема и продолжительности лечения, вида хирургического вмешательства, необходимых препаратов и других процедур. Играет роль ценовая политика клиники. Дешевое лечение не всегда бывает оптимальным: врач может работать по устаревшим протоколам, использовать не самые эффективные препараты.
В Европейской онкологической клинике можно получить лечение на уровне ведущих западных онкологических центров по более низкой стоимости.
источник
 Формирование данного симптома может привести к истощению человека, из-за невозможности потреблять достаточный объём пищи. Такой показатель характерен для совмещения лучевой и химической терапии. Для этого случая доктор советует искусственное поступление еды, для поддержания массы тела. Также поступают медикаменты и жидкость. Искусственное питание позволяет контролировать вес, предоставляет нужное количество воды, снижает давление. Для осуществления поступления пищи в организм используют тонкую трубку, которая проходит через нос или делается отверстие в коже. Такое питание позволяет не прекращать терапию из-за снижения веса.
Формирование данного симптома может привести к истощению человека, из-за невозможности потреблять достаточный объём пищи. Такой показатель характерен для совмещения лучевой и химической терапии. Для этого случая доктор советует искусственное поступление еды, для поддержания массы тела. Также поступают медикаменты и жидкость. Искусственное питание позволяет контролировать вес, предоставляет нужное количество воды, снижает давление. Для осуществления поступления пищи в организм используют тонкую трубку, которая проходит через нос или делается отверстие в коже. Такое питание позволяет не прекращать терапию из-за снижения веса.